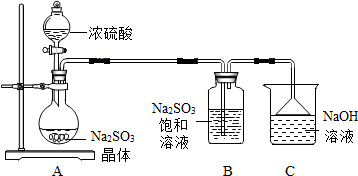
题目内容
10.某化学兴趣小组的同学要探究铝、铁、铜三种金属的活动性顺序,请你参与探究并填写空格.【实验探究】同学们将粗细相同的、打磨过的铝丝和铁丝分别插入硫酸亚铁溶液、硫酸铜溶液中:
| 操作 | 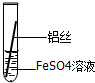 甲 | 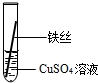 乙 | 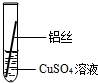 丙 | 根据现象得出金属活动性顺序 |
| 现象 | 铝丝表面附着银白色固体 | 铁丝表面附着红色固体 | 铝丝表面附着红色固体 | Al>Fe>Cu |
【交流讨论】
(1)同学们经讨论后认为上述方案可以优化,丙(选填“甲”、“乙”或“丙”)试管的实验时多余的.
(2)洁洁认为,只用一支盛有少量稀硫酸的试管,合理安排金属丝的插入顺序(能与稀硫酸反应的要一次将稀硫酸消耗完),也能证明铁、铝、铜这三种金属的活动性顺序.他设计了两种插入顺序,请你补全顺序二:
顺序一:Cu Fe Al
顺序二:Fe Cu Al.
洁洁按顺序一做实验时,发现铁丝放入稀硫酸中片刻后无气泡产生,几分钟后才有少量气泡产生,你认为可能的原因是铁丝生锈,没有打磨.
【拓展迁移】为了回收金属,同学们将甲、乙、丙三支试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物和滤液.向不溶物中加稀硫酸,有气泡产生,则不溶物中一定含有铜和铁.
分析 【实验探究】根据金属活动性只有排在前面的金属才能把后面的金属从它的盐溶液中置换出来;化学方程式的书写主要做好以下几个方面:反应物、生成物、反应条件、化学式的书写、配平、沉淀气体的标注等;
【交流讨论】(1)根据探究实验的设计进行分析;
(2)根据金属活动性进行分析;
根据铁生锈进行分析;
【拓展迁移】根据三种金属的活动性进行分析.
解答 解:【实验探究】铝丝表面附着银白色固体,说明铝能置换出铁,证明铝的活动性比铁强,铁丝伸入硫酸铜中铁丝表面有红色物质析出,说明铁的活动性比铜强,因此,Al>Fe>Cu;
铝与硫酸铜溶液反应的化学方程式2Al+3CuSO4=Al2(SO4)3+3Cu;
【交流讨论】(1)由甲证明铝的活动性比铁强,由乙说明铁的活动性比铜强,因此,Al>Fe>Cu,所以不需丙实验,故选丙;
(2)只有一支盛有少量稀盐酸的试管,先插入铁片,铁片表面产生气泡,溶液中再伸入铜片无现象,因为铜不能与氯化亚铁反应,再伸入铝片时,不产生气泡因为盐酸消耗完了,但是铝的活动性比铁强,铝的表面会析出金属铁;也能证明三种金属的活动性强弱;故填:Fe Cu Al;
铁丝放入稀硫酸中片刻后无气泡产生,几分钟后才有少量气泡产生,可能铁丝生锈,硫酸先和表面的氧化铁反应,再和铁反应,故填:铁丝生锈,没有打磨;
【拓展迁移】将甲、乙、丙三支试管中反应后的物质倒入同一大烧杯中,一段时间后过滤,得到不溶物和滤液.根据三种金属的活动性,一定能置换出铜,可能有铁,而向不溶物中加稀硫酸,有气泡产生,则证明一定有铁,故填:铜和铁;
故答案为:【实验探究】Al>Fe>Cu;2Al+3CuSO4=Al2(SO4)3+3Cu;
【交流讨论】(1)丙;
(2)Fe Cu Al;
铁丝生锈,没有打磨;
【拓展迁移】铜和铁.
点评 本题主要考查金属的活动性,注意只有排在前面的金属才能把后面的金属从它的盐溶液中置换出来.

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案| A. | 硫-单质 | B. | 纯碱-碱 | C. | 酒精-有机化合物 | D. | 生石灰-氧化物 |
| A. | 金刚石刀切割玻璃 | B. | 用粮食发酵酿酒 | ||
| C. | 生石灰吸水变成粉末 | D. | 铁矿石在高炉中炼铁 |
【提出问题久置“双吸剂”固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下会发生如下反应:Fe+2FeCl3═3X,X的化学式为FeCl2;
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.久置固体中可能含有Ca(OH)2的原因是CaO+H2O═Ca(OH)2 (用化学方程式表示).
【实验探究】下表是小昊设计的实验方案和记录的实验报告,请你补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量固体放于试管中,加入蒸馏水充分搅拌 | 用手触摸试管,试管外壁发烫 | 固体中一定含有氧化钙 |
| ②另取少量固体放于试管中,滴加足量稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有铁,一定不含Fe2O3 |
| ③将步骤②中产生的气体通入澄清的石灰水中 | 澄清石灰水变浑浊 | 固体中一定含有CaCO3 |
| A. | 锰钢 | B. | 红磷 | C. | 五氧化二磷 | D. | 硝酸钾 |
| A. | 点燃H2、CO等可燃性气体可能会发生爆炸 | |
| B. | 用乙醇汽油作汽车燃料,不能节能减排 | |
| C. | 用水灭火,主要是降低了可燃物的着火点 | |
| D. | 石油是一种化工产品 |