题目内容
11.读下表完成填空| 元素符号 | A | B | C | D |
| 该元素的某 微粒结构图 | 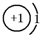 |  | 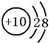 | 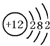 |
(2)化学性质比较稳定的原子是BD.
(3)在表中属于阴离子的是B.
(4)由表中各元素的结构示意图,我发现:不同种元素的质子数不同.
(5)MgF2中Mg的化合价为-1.
分析 若粒子的最外层电子数为8(氦为2个),属于相对稳定结构;若原子的最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子;据此进行分析解答.根据物质的化学式MgF2,利用化合物中各元素的化合价代数和为0的原则,由化合物中Mg元素为+2价,计算化合物中F元素的化合价.
解答 解:
(1)由原子结构示意图可知:原子序数为1的氢元素的其最外层电子数是1,在化学反应中易失去1个电子而形成氢离子,原子序数为12的镁元素的其最外层电子数是2,在化学反应中易失去2个电子而形成阳离子;
(2)四种原子中,B最外层电子数为8,属于相对稳定结构,化学性质比较稳定;
(3)B中质子数<电子数,属于阴离子;
(4)元素的种类是由质子数决定的,不同种元素的质子数不同;
(5)设化合物MgF2中F元素化合价为n价,依化合物中各元素化合价代数和为零的原则,有(+2)×1+n×2=0,解之得n=-1;
故答案为:
(1)AD;
(2)BD;
(3)B;
(4)质子数;
(5)-1.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,明确原子结构示意图中最外层电子数与得失电子的关系是解题的关键.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案
相关题目
2.经测定钒(V)的核内有28个中子,核外有23个电子,其氯化物的相对分子质量为228.5,若钒在氧化物和氯化物中化合价相同,则钒的氧化物的化学式为( )
| A. | VO2 | B. | V2O | C. | V2O5 | D. | VO |
6.为了预防缺铁性贫血,人体必须保证足够的铁的摄入.这里的“铁”是指( )
| A. | 铁单质 | B. | 氧化铁 | C. | 铁元素 | D. | 铁原子 |
3.不同种元素最本质的区别是( )
| A. | 质子数不同 | B. | 最外层电子数不同 | ||
| C. | 中子数不同 | D. | 相对原子质量不同 |
20.航空航天材料中的重要金属用Si反应来制取,反应的化学方程式为:TiO2+Si═SiO2+Ti,则该反应属于化学反应基本类型中的( )
| A. | 化合反应 | B. | 置换反应 | C. | 分解反应 | D. | 复分解反应 |
 .
.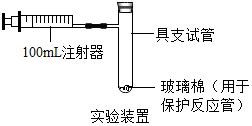 如图是某同学设计的测定空气中氧气含量的实验装置.在具支试管中铺上一层玻璃棉,用于保护反应管;注射器提前连接好,装入100mL水.实验时,将橡皮塞取下,取一定量的白磷放入具支试管底部的玻璃棉上,塞紧橡皮塞(并用拇指压住),在试管底部稍微加热,白磷燃烧.
如图是某同学设计的测定空气中氧气含量的实验装置.在具支试管中铺上一层玻璃棉,用于保护反应管;注射器提前连接好,装入100mL水.实验时,将橡皮塞取下,取一定量的白磷放入具支试管底部的玻璃棉上,塞紧橡皮塞(并用拇指压住),在试管底部稍微加热,白磷燃烧. 新药左旋氧氟沙星(C18H20FN3O4)可用于治疗敏感菌引起的呼吸道感染,其说明书中部分内容如图.
新药左旋氧氟沙星(C18H20FN3O4)可用于治疗敏感菌引起的呼吸道感染,其说明书中部分内容如图.