题目内容
(1)为了探究物质在溶解时溶液温度的变化,请你设计一种实验装置来进行探究,画出装置图,并简要说明.
(2)欲探究铁.银.铜的活泼性,最佳方案是
A.将铁银分别加入到硫酸铜溶液中B.将铁铜分别加入到硝酸银溶液中
C将铁铜银分别加入到稀盐酸中.
(2)欲探究铁.银.铜的活泼性,最佳方案是
A.将铁银分别加入到硫酸铜溶液中B.将铁铜分别加入到硝酸银溶液中
C将铁铜银分别加入到稀盐酸中.
考点:溶解时的吸热或放热现象,金属活动性顺序及其应用
专题:溶液、浊液与溶解度,金属与金属材料
分析:(1)根据物质溶于水温度的变化,影响一定装置中的气体压强考虑;
(2)根据金属活动性顺序和金属单质与可溶性盐反应的规律进行解答,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
(2)根据金属活动性顺序和金属单质与可溶性盐反应的规律进行解答,在金属活动性顺序中,氢前的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来.
解答:解:(1)我们可设计右图所示装置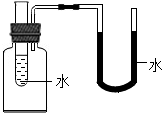 ,右侧U型管中的液面发生明显变化,说明与U型管相连通的广口瓶内气体体积受到小试管加入物质的影响而发生变化.也就是说,向小试管内加入一定量物质时,放出了大量热量或吸收了大量热量,使得试剂瓶中气体的体积膨胀或收缩.
,右侧U型管中的液面发生明显变化,说明与U型管相连通的广口瓶内气体体积受到小试管加入物质的影响而发生变化.也就是说,向小试管内加入一定量物质时,放出了大量热量或吸收了大量热量,使得试剂瓶中气体的体积膨胀或收缩.
(2)A、铁能置换出硫酸铜中的铜,说明铁比铜活泼,银不能置换出硫酸铜中的铜.说明铜比银活泼,故A正确;
B、铁和铜都能置换出硝酸银中的银,说明铁和铜在银的前面,无法比较铁和铜的活泼性,故B错误;
C、铁能与盐酸反应生成氢气,说明铁在氢的前面,铜和银都不能和盐酸反应,说明铜和银都在铁的后面,无法比较铜和银的活泼性强弱,故C错误;
故答案为:(1) (2)A
(2)A
 ,右侧U型管中的液面发生明显变化,说明与U型管相连通的广口瓶内气体体积受到小试管加入物质的影响而发生变化.也就是说,向小试管内加入一定量物质时,放出了大量热量或吸收了大量热量,使得试剂瓶中气体的体积膨胀或收缩.
,右侧U型管中的液面发生明显变化,说明与U型管相连通的广口瓶内气体体积受到小试管加入物质的影响而发生变化.也就是说,向小试管内加入一定量物质时,放出了大量热量或吸收了大量热量,使得试剂瓶中气体的体积膨胀或收缩.(2)A、铁能置换出硫酸铜中的铜,说明铁比铜活泼,银不能置换出硫酸铜中的铜.说明铜比银活泼,故A正确;
B、铁和铜都能置换出硝酸银中的银,说明铁和铜在银的前面,无法比较铁和铜的活泼性,故B错误;
C、铁能与盐酸反应生成氢气,说明铁在氢的前面,铜和银都不能和盐酸反应,说明铜和银都在铁的后面,无法比较铜和银的活泼性强弱,故C错误;
故答案为:(1)
 (2)A
(2)A点评:此题考查的是学科综合题,考查了理化方面的知识.在学习中,要把握好各方面的知识.
同学们要会利用金属活动顺序表设计实验,去验证金属的活动性强弱,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.
同学们要会利用金属活动顺序表设计实验,去验证金属的活动性强弱,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案
相关题目
吸烟有害健康的原因之一是香烟燃烧产生的物质中,含有使血红蛋白不能很好地跟氧气结合的有毒气体是( )
| A、一氧化碳 | B、氮气 |
| C、二氧化碳 | D、二氧化硫 |
下列应用的原理用化学方程式表示错误的是( )
| A、电解水:H2O=H2↑+O2↑ | ||||
B、铝在氧气中燃烧:4Al+3O2
| ||||
C、高温煅烧石灰石制取生石灰CaCO3
| ||||
D、用红磷燃烧测定空气中氧气含量4P+5O2↑
|

 (1)小明同学课下自制了如图的实验装置,对水通电分解进行了实验探究,请你和他一起完成此实验.
(1)小明同学课下自制了如图的实验装置,对水通电分解进行了实验探究,请你和他一起完成此实验.