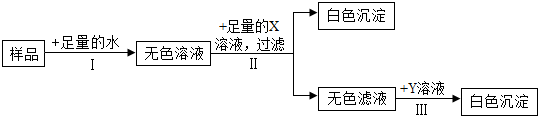
题目内容
20.晾晒海水得到的粗盐中往往含有可溶性盐如 CaCl2、Na2SO4以及不溶性的泥沙等杂质,必须经过分离、提纯后才能用于人们的生活,以下是粗盐提纯的操作流程: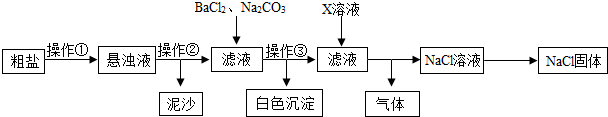
根据上述过程回答下列问题:
(1)操作①~③均会用到的玻璃仪器是玻璃棒,它在操作③的作用是引流.
(2)白色沉淀中含有的物质是CaCO3、BaSO4、BaCO3.
(3)X 溶液是(写名称),加入适量 X 溶液的目的是除去过量的Na2CO3.
(4)小刚同学认为该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,请你为他找出该方案所有会生成氯化钠的化学方程式:Na2CO3+BaCl2=BaCO3↓+2NaCl、Na2SO4+BaCl2=BaSO4↓+2NaCl、Na2CO3+2HCl=2NaCl+H2O+CO2↑.
分析 (1)根据各步操作的目的及仪器、作用分析;
(2)根据各反应的产物结合除杂的步骤分析;
(3)根据产生氯化钠的途径结合各步实验目的分析写出反应的方程式.
解答 解:(1)操作①将粗盐溶于水,因此操作是溶解;操作②是将泥沙和溶液分离,因此操作是过滤;操作③是将沉淀和滤液分离,因此操作是过滤,各操作中都会用到玻璃棒,其中过滤中玻璃棒起到引流的作用;
故答案为:玻璃棒;引流;
(2)氯化钡和硫酸钠反应产生硫酸钡沉淀和氯化钠,碳酸钠和氯化钙反应产生碳酸钙沉淀和氯化钠,和氯化钡反应产生碳酸钡沉淀和氯化钠,因此沉淀有硫酸钡、碳酸钡、碳酸钙;
故答案为:CaCO3、BaSO4、BaCO3;
(3)X溶液是除去过量的碳酸钠,为了不增加新的杂质,因此X是稀盐酸;
故答案为:稀盐酸,除去过量的 Na2CO3
(4)该方案实际得到的氯化钠的途径有:氯化钡和硫酸钠反应产生硫酸钡沉淀和氯化钠,碳酸钠和氯化钙反应产生碳酸钙沉淀和氯化钠,和氯化钡反应产生碳酸钡沉淀和氯化钠,碳酸钠和盐酸反应产生氯化钠、水和二氧化碳;
故答案为:Na2SO4+BaCl2=BaSO4↓+2NaCl、Na2CO3+BaCl2=BaCO3↓+2NaCl、Na2CO3+CaCl2=CaCO3↓+2NaCl、Na2CO3+2HCl=2NaCl+H2O+CO2↑.
点评 本题考查是物质的除杂和净化的知识,对于培养同学们的分析判断和整合能力很有帮助,解题时依据实验的目的及除杂的方法进行分析,并熟练书写反应的方程式.

练习册系列答案
相关题目
8.“84”消毒液的主要成分是次氯酸钠,是烧碱溶液与物质X反应得到的,反应方程式如下:
2NaOH+X═NaClO+NaCl+H2O 则X的化学式是( )
2NaOH+X═NaClO+NaCl+H2O 则X的化学式是( )
| A. | HCl | B. | Cl2 | C. | ClO2 | D. | HClO |
5.通过分析下列各组对比实验观察到的正常现象,能得到相应结论的是( )
| 实验方案 | 实验结论 | ||
| 实验1 | 实验2 | ||
| ① | 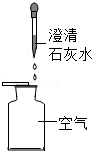 | 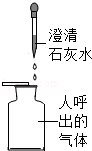 | 人呼出的气体中CO2的含量高于空气 |
| ② |  | 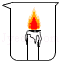 | 燃烧需要可燃物的温度达到着火点 |
| ③ | 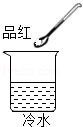 | 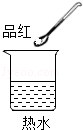 | 温度升高,分子运动加快 |
| ④ | 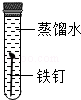 | 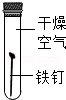 | 铁生锈需要氧气和水 |
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
12.下列关于生活和健康常识的说法不正确的是( )
| A. | 用碳酸氢钠焙制糕点 | |
| B. | 饮用牛奶和豆浆可以缓解重金属引起的中毒 | |
| C. | 医疗上用酒精杀菌消毒 | |
| D. | 用甲醛溶液对水产品保鲜 |
 如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11.0g,放入烧杯中加水完全溶解后滴加上述配制的盐酸溶液至完全反应,最后测得生成气体的质量为4.4g,计算:
如图是配制好的盐酸溶液的标签,请根据标签上的文字信息,进行计算:某纯碱样品中含有少量氯化钠.为测定样品中碳酸钠的质量分数,现称取该样品11.0g,放入烧杯中加水完全溶解后滴加上述配制的盐酸溶液至完全反应,最后测得生成气体的质量为4.4g,计算: