题目内容
7.为了除去铜粉中混有的铁粉,并用提纯的铜粉制取胆矾(CuSO4•5H2O).某课外活动小组的同学按如下流程进行实验.(反应中部分生成物已略去)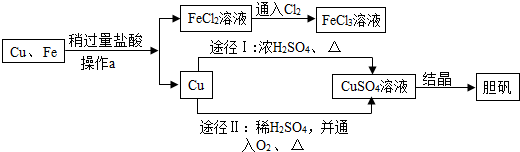
已知:Cu+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CuSO4+SO2↑+2H2O回答下列有关问题:
(1)操作a的名称是过滤;除去铜粉中的铁粉,最简便的实验方法是用磁铁吸引.
(2)FeCl2溶液中通入Cl2发生化合反应,写出该反应的化学方程式2FeCl2+Cl2=2FeCl3.
(3)由Cu制CuSO4溶液的途径Ⅱ中,若不通入O2,反应将不会发生,原因是在金属活动顺序中,铜是位于氢之后的,与稀硫酸不反应.途径Ⅱ与途径Ⅰ相比较,其显著的优点是不会产生污染空气的二氧化硫气体(回答一点即可).
(4)FeCl3溶液可腐蚀铜以制作印刷线路板,反应只生成两种常见的盐,则该反应的化学方程式为2FeCl3+Cu═2FeCl2+CuCl2.
分析 (1)根据分离混合物的方法以及铁的性质来分析;
(2)根据反应的原理及其类型来分析;
(3)根据铜的化学性质来分析;根据反应的原理、条件来分析;
(4)根据反应的原理来分析.
解答 解:(1)操作a是用来分离固体与液体的方法,是过滤;铁可以被磁铁吸引,而铜不会,所以可用磁铁吸引的方法除去铜粉中混有的铁粉;故填:过滤;用磁铁吸引;
(2)氯化亚铁与氯气反应生成氯化铁;故填:2FeCl2+Cl2=2FeCl3;
(3)在金属活动顺序中,铜排在H后面,与硫酸不反应;铜与浓硫酸的反应中会产生有毒的二氧化硫气体而污染空气;故填:在金属活动顺序中,铜是位于氢之后的,与稀硫酸不反应;不会产生污染空气的二氧化硫气体;
(4)氯化铁与铜反应生成氯化亚铁和氯化铜;故填:2FeCl3+Cu═2FeCl2+CuCl2.
点评 本题考查了工业生产印刷线路板,从废液中回收铜并得到FeCl3溶液循环利用的原理分析和反应判断,熟练利用金属活动性顺序,提纯和回收利用金属;会处理实验流程图是解题的关键.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
17.用三块相同的铝片(均已去除氧化膜)进行如下实验.
实验①:取第一块铝片,放入稀硫酸中,有明显的现象;
实验②:取第二块铝片,放入CuSO4溶液中,铝片表面有红色物质析出;
实验③:取第三块铝片,放入浓硫酸中,竟然没有明显的现象;
实验④:将实验③中的铝片取出,洗净后放入CuSO4溶液中,也没有明显现象.
下列说法不正确的是( )
实验①:取第一块铝片,放入稀硫酸中,有明显的现象;
实验②:取第二块铝片,放入CuSO4溶液中,铝片表面有红色物质析出;
实验③:取第三块铝片,放入浓硫酸中,竟然没有明显的现象;
实验④:将实验③中的铝片取出,洗净后放入CuSO4溶液中,也没有明显现象.
下列说法不正确的是( )
| A. | 铝片与浓硫酸不能发生化学反应 | B. | 实验①观察到铝片表面有气泡产生 | ||
| C. | 由实验②可以得出金属铝比铜活泼 | D. | 浓硫酸与稀硫酸的化学性质有差别 |
18.推理是一种重要的学习方法.下列推理中正确的是( )
| A. | 碳酸盐遇酸有气泡产生,则加酸产生气泡的物质一定是碳酸盐 | |
| B. | 单质是由一种元素组成的,则由一种元素组成的物质一定是单质 | |
| C. | 某物质完全燃烧,生成物只有CO2和H2O,该物质一定由C、H、O三种元素组成 | |
| D. | 元素是具有相同核电荷数的原子的总称,则有相同核电荷数的原子一定属于同种元素 |
2.某化学兴趣小组在探究稀盐酸的化学性质时,做了如图一所示的三个实验.
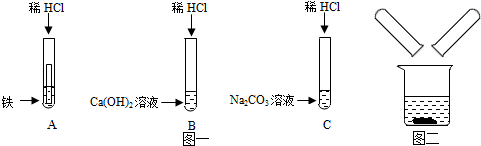
(1)A试管中的反应现象是铁片表面有气泡产生,溶液由无色逐渐变为浅绿色.
(2)C试管中反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:有NaCl
乙同学猜想:有NaCl、CaCl2
丙同学猜想:有NaCl、CaCl2、HCl
你的猜想:有NaCl、Na2CO3.
【交流讨论】
你认为丙同学的猜想一定不正确,理由是Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀.
【设计实验】请设计实验证明你的猜想正确.
【反思与总结】判断反应后溶液中溶质的成分,除要考虑生成物外,还需考虑反应物是否有剩余(表述合理即可)..

(1)A试管中的反应现象是铁片表面有气泡产生,溶液由无色逐渐变为浅绿色.
(2)C试管中反应的化学方程式是Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)实验结束后,小组同学将B、C两支试管中的废液同时倒入一个洁净的烧杯中(如图二所示),观察到先有气泡产生,后有白色沉淀生成.同学们将烧杯内的物质进行过滤,对所得滤液的溶质成分进行探究.
【提出猜想】
甲同学猜想:有NaCl
乙同学猜想:有NaCl、CaCl2
丙同学猜想:有NaCl、CaCl2、HCl
你的猜想:有NaCl、Na2CO3.
【交流讨论】
你认为丙同学的猜想一定不正确,理由是Na2CO3先和HCl反应,当HCl过量时,Na2CO3被完全反应,不可能再与CaCl2反应生成白色沉淀.
【设计实验】请设计实验证明你的猜想正确.
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,向其中滴加无色酚酞试液. | 溶液变红. | 我的猜想成立 |
19.下列反应属于复分解反应的是( )
| A. | 碳酸钙与盐酸反应 | B. | 加热高锰酸钾 | ||
| C. | 氧化钙与水反应 | D. | 碳与氧化铜反应 |
17.下列各组物质中,均属于纯净物的是( )
| A. | 合成纤维、维生素 | B. | 天然气、水银 | C. | 冰水混合物、干冰 | D. | 液态氮、碘盐 |
 Ⅰ.今年湄公河流域遭遇百年干旱,中国克服困难伸援手开闸放水,使湄公河沿岸的早情得到极大缓解.请回答下列问题:
Ⅰ.今年湄公河流域遭遇百年干旱,中国克服困难伸援手开闸放水,使湄公河沿岸的早情得到极大缓解.请回答下列问题: