题目内容
17.质量分数为10%的KNO3溶液100g.(1)加入10g KNO3固体,完全溶解,溶质的质量分数为多少?
(2)蒸发掉50g水,溶质的质量分数为多少?
分析 本题考查基础的溶质的质量分数的计算公式,以及公式的转化运用:
(1)根据混合前溶质的质量之和等于混合后溶液中的溶质的质量来计算;
(2)根据蒸发时溶质的质量不变来计算.
解答 解:(1)因为加入的溶质的质量为10g,而溶质的质量分数=$\frac{溶质质量}{溶液质量}$×100%,溶质质量=溶液的质量×溶质质量分数;
故加入10gKNO3固体,完全溶解,溶质的质量分数为$\frac{10g+100g×10%}{100g+10g}$≈18.2%;
(2)因为蒸发水的质量为50g,由蒸发前后溶质的质量不变,则$\frac{100g×10%}{100g-50g}$×100%=20%;
故答案为:(1)18.2%;(2)20%.
点评 本题考查增大溶质质量分数的方法及有关计算,明确溶液中的变化并学会利用溶质的质量关系来列等式计算是解答的关键.

练习册系列答案
 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案
相关题目
8.人体健康与化学物质和元素含量有密切联系,下列有关做法正确的是( )
| A. | 甲醛是重要的防腐剂,为了防止食品变质腐烂,我们可以用甲醛溶液来浸泡食品 | |
| B. | 为了响应“节能减排”,霉变食物应高温蒸煮后再食用 | |
| C. | “大自然”牌蔬菜,天然种植,不含任何元素,真正的“绿色”食品 | |
| D. | 缺铁会导致缺铁性贫血,人们可以食用加入铁强化剂的酱油来预防 |
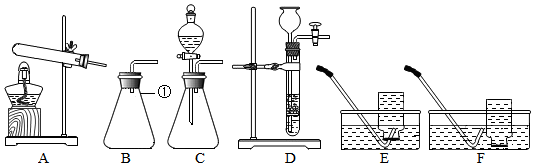
5.下列实验操作中不正确的是( )
| A. |  洗涤试管 | B. | 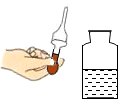 取出液体 | ||
| C. | 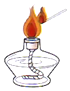 点燃酒精灯 | D. | 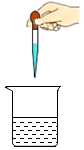 滴加液体 |
3.下列化肥中不属于氮肥的是( )
| A. | NH4HCO3 | B. | CO(NH2)2 | C. | NaNO3 | D. | NaCl |
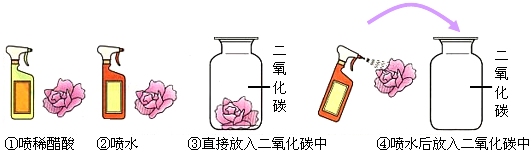
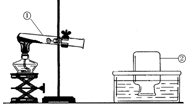 绘制实验装置图是我们初中生应该掌握的一项技能.如图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.请按要求回答下列问题.
绘制实验装置图是我们初中生应该掌握的一项技能.如图是某同学正在绘制的实验室用高锰酸钾制取氧气的装置图.请按要求回答下列问题.