题目内容
18.甲和乙反应生成丙和丁的围观示意图如下,则下列说法中不正确的是( )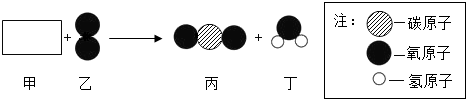
| A. | 甲物质的化学式为CH2O | |
| B. | 除甲以外其他物质都是氧化物 | |
| C. | 生成的丙、丁两物质的质量比是22:9 | |
| D. | 反应前后分子个数不变 |
分析 根据化学反应前后原子的种类、数目都不变分析甲的元素组成,根据氧化物的定义结合乙的微观示意图分析乙的属类,根据物质的质量比计算,据此逐项分析
解答 解:A、甲的化学式可能是CH2O,和氧气反应产生二氧化碳和水,符合微观示意图的反应关系,故选项正确;
B,乙分子是两个氧原子构成的氧分子,因此属于单质,故选项错误;
C、生成物是二氧化碳和水,由于不确定甲的化学式,因此无法确定二者的质量比,故选项错误;
D、由微粒的变化可知,反应前后分子的种类发生了改变,故选项错误.
故选:A.
点评 本题为微观示意图的考查,了解微粒观点及模型图的应用及依据质量守恒定律进行相关计算是解题的关键.

练习册系列答案
相关题目
8.拉瓦锡曾将少量汞放在密闭容器里,加热十二天后,部分液态汞变成了红色氧化汞粉末,容器里空气体积减少了约 $\frac{1}{5}$.另将红色粉末加强热,得到汞和一种气体,该气体的体积恰好等于原来密闭容器里减少的空气体积.由实验得出的说法不正确的是( )
| A. | 红色粉末是汞与氧气发生化合反应生成的氧化汞 | |
| B. | 证明了空气中氧气约占总体积的$\frac{1}{5}$,氮气占 $\frac{4}{5}$ | |
| C. | 通过改变反应条件可使某些反应向反方向进行 | |
| D. | 测定结果比用木炭燃烧测空气中氧气含量更准确 |
13.实验与探究是化学学习的重要方法和内容,李明看到家里多年未用的铜制火锅上有绿色的锈迹,他对绿色锈迹的成分和性质产生了浓厚兴趣.
【查阅资料】
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解;
②无水硫酸铜为白色粉末,遇水变蓝;
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中.
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成.
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体成分.
【猜想与假设】该黑色固体可能是①碳粉;②氧化铜;③碳和氧化铜的混合物.
【设计方案】请帮助该同学完成下述实验报告:
探究二:碱式碳酸铜受热分解还会生成CO2和H2O.
【进行实验】选择如下图所示装置进行验证
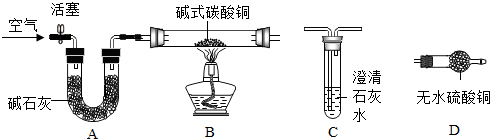
步骤一:连接A和B,打开活塞,通入一段时间的空气;
步骤二:点燃酒精灯,依次连接装置A→B→D→C(填“C”,“D”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热
【解释与结论】
①当观察到C中石灰水变浑浊,D中无水硫酸铜变蓝,说明碱式碳酸铜受热分解生成了CO2和H2O,写出装置C中反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O;
②写出Cu2(OH)2CO3受热分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
【反思与评价】
上述装置中A的作用是除去空气中的水分和二氧化碳,防止对产物的检验造成干扰.
【查阅资料】
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解;
②无水硫酸铜为白色粉末,遇水变蓝;
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中.
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成.
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体成分.
【猜想与假设】该黑色固体可能是①碳粉;②氧化铜;③碳和氧化铜的混合物.
【设计方案】请帮助该同学完成下述实验报告:
| 实验操作与现象 | 实验结论 |
| 取黑色粉末,加入足量稀硫酸,充分反应后,黑色固体全部溶解形成蓝色溶液 | 猜想②正确 |
【进行实验】选择如下图所示装置进行验证

步骤一:连接A和B,打开活塞,通入一段时间的空气;
步骤二:点燃酒精灯,依次连接装置A→B→D→C(填“C”,“D”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热
【解释与结论】
①当观察到C中石灰水变浑浊,D中无水硫酸铜变蓝,说明碱式碳酸铜受热分解生成了CO2和H2O,写出装置C中反应的化学方程式CO2+Ca(OH)2=CaCO3↓+H2O;
②写出Cu2(OH)2CO3受热分解的化学方程式Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+H2O+CO2↑.
【反思与评价】
上述装置中A的作用是除去空气中的水分和二氧化碳,防止对产物的检验造成干扰.
10.“NaCl+CO2+NH3+H2O═NaHCO3+NH4Cl”是著名的“侯氏制碱法”的重要反应,下列有关叙述正确的是( )
| A. | NaHCO3是纯碱 | |
| B. | 析出晶体后剩余溶液中溶质只有NH4Cl | |
| C. | 配制饱和食盐水时,可通过搅拌来提高食盐的溶解度 | |
| D. | 向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收 |
8.下列选项中关于水的说法正确的是( )
| A. | 生活中采取蒸馏的方法将硬水软化 | |
| B. | 液态水转化为水蒸气,水分子体积增大 | |
| C. | 电解水得到的氢气和氧气质量比约为2:1 | |
| D. | 保持水的化学性质的最小粒子是水分子 |
 有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应“→”表示物质之间的转化关系.
有关物质之间的部分转化关系如图所示.其中“-”表示物质之间能发生化学反应“→”表示物质之间的转化关系.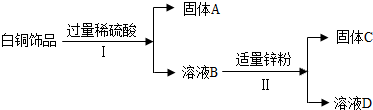 白铜(Cu、Ni合金)因为光泽好、耐腐蚀、容易加工等优点,常代替银做饰品.如图所示是某实验室分离废弃白铜饰品成分的流程(部分反应产物在图中已略去).
白铜(Cu、Ni合金)因为光泽好、耐腐蚀、容易加工等优点,常代替银做饰品.如图所示是某实验室分离废弃白铜饰品成分的流程(部分反应产物在图中已略去).