题目内容
4.溶解是生活中常见的现象,不同物质在水中的溶解能力不同.用硫酸铜进行如图所示的实验,观察后完成下列填空(用编号表示)

(1)硫酸铜的溶解度随温度升高变大(填“变大”或“不变”或“变小”).
(2)所得三个溶液中:一定属于饱和溶液的是A,溶液中溶质质量的大小关系是B=C>A.
分析 (1)由图示知,硫酸铜的溶解度随温度升高而升高;
(2)根据饱和溶液的判断方法,以及溶液中溶质的质量进行分析.
解答 解:(1)由图示知,硫酸铜的溶解度随温度升高而升高;
(2)通过分析可知,A烧杯底部有固体,所以一定属于饱和溶液的是A,A中的溶质有剩余,B、C中的溶质分别为mg,所以溶液中溶质质量的大小关系是:B=C>A.
故答案为:(1)变大;
(2)A;B=C>A.
点评 本题难度不大,掌握理解溶解度的概念并能灵活运用是正确解答本题的关键.

练习册系列答案
相关题目
6.下列对物质的分类不正确的是( )
| A. | 碱:烧碱、纯碱 | B. | 有机物:甲烷、乙醇 | ||
| C. | 氧化物:冰水共存物、干冰 | D. | 复合肥料:硝酸钾、磷酸二氢铵 |
7.打火机的主要燃料是丁烷(C4H10),有关于丁烷的说法不正确的是( )
| A. | 具有可燃性 | |
| B. | 完全燃烧只生成水 | |
| C. | 碳、氢元素的质量比为24:5 | |
| D. | 一个分子由4个碳原子和10个氢原子构成 |
4.如图就金属与盐酸反应的探究实验.下列说法错误的是( )


| A. | 甲可能是Mg | |
| B. | 丁说,我是黄铜,我不怕酸 | |
| C. | 将乙放在丙的盐溶液中可以置换出丙 | |
| D. | 四种金属的活动性顺序是:甲>乙>丙>丁 |
16.化学学习中经常会遇到一些“相等”,下列有关“相等”的说法中错误的是( )
| A. | 化学反应前后原子的总数一定相等 | |
| B. | 催化剂在反应前后质量一定相等 | |
| C. | 中和反应中参加反应的酸和碱的质量一定相等 | |
| D. | 溶液稀释前后溶质的质量一定相等 |
13.区分下列物质的两个实验方案都合理的是( )
| 选项 | 需区分的物质 | 方案一 | 方案二 |
| A | 硫酸铵和氯化钾 | 加熟石灰,研磨 | 观察状态 |
| B | 聚乙烯和聚氯乙烯 | 点燃,闻气味 | 加热观察是否熔化 |
| C | 大理石和碳酸钠粉末 | 取样,分别加入足量稀盐酸 | 取样,分别加入足量水 |
| D | 木炭和氧化铜 | 观察颜色 | 通入CO加热 |
| A. | A | B. | B | C. | C | D. | D |
14.下列物质间的转化,不能一步实现的是( )
| A. | Fe(OH)3→FeCl3 | B. | Fe→Fe2(SO4)3 | C. | CO2→CaCO3 | D. | MgCl2→KCl |
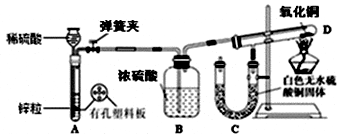
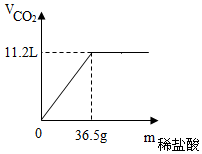 80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如图所示.试回答:
80g石灰石样品与稀盐酸反应制取二氧化碳气体,反应产生的二氧化碳气体的体积与加入的稀盐酸的质量关系如图所示.试回答: