题目内容
1.科技节活动中,化学实验小组做了如下实验,请回答以下问题.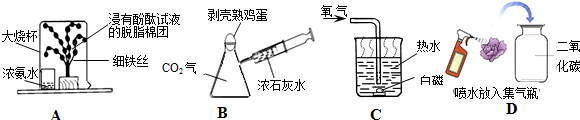
(1)图A所示实验可观察到“铁树”上浸有无色酚酞试液的棉团由白色变为红色,该实验中没有涉及的性质是B(填字母).
A.氨分子是不断运动的 B.氨分子有一定质量 C.浓氨水具有挥发性
(2)图B所示实验,将注射器中浓石灰水注入瓶中,会看到鸡蛋被“吞”入瓶中,该实验中涉及的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O.
(3)图C所示实验,当通过导管向热水中通入氧气时,白磷在水下燃烧,该实验说明燃烧需要的条件为:①可燃物;②达到燃烧所需要的最低温度;③与氧气接触,反应的化学方程式为4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5.
(4)图D所示实验观察到紫色小花变为红色,小花变红的原因是二氧化碳能与水反应生成碳酸,碳酸能使石蕊变红(用化学方程式表示)CO2+H2O=H2CO3.
【综合应用】“水火不相容”是指水能灭火,其实水有时也可以“生火”,比如钾遇水会立刻着火,钾遇水生成H2和KOH,该反应是放热(填“吸热”或“放热”)反应,其反应化学方程式为2K+2H2O═2KOH+H2↑.
分析 (1)从①浓氨水具有挥发性,挥发出的氨气是由氨分子构成的;②酚酞试液是一种酸碱指示剂,遇酸不变色,遇碱变红色;③氨水是碱性的,能够使酚酞试液变红;④保持物质化学性质的最小粒子是分子,保持氨气的化学性质的最小粒子是氨分子分析解答;
(2)考虑二氧化碳气体能和浓氢氧化钙溶液迅速反应,装置内气压减小解释现象;
(3)从白磷能在水下燃烧,其实质是白磷和氧气反应生成了五氧化二磷,能在水下燃烧,说明满足燃烧的条件去分析解答;
(4)根据二氧化碳的水溶液呈酸性,能使石蕊试液变红分析.
【综合应用】燃烧所需要温度达到着火点,钾的燃烧说明反应放出了热量使钾的温度升高至着火点;钾与水发生置换反应,生成氢气和碱氢氧化钾.
解答 解:(1)①浓氨水具有挥发性,挥发出的氨气是由氨分子构成的;②酚酞试液是一种酸碱指示剂,遇酸不变色,遇碱变红色;③氨水是碱性的,能够使酚酞试液变红;④由于分子是不断运动的,当氨分子运动到浸有无色酚酞试液的棉团时,和酚酞试液观接触,由于保持物质化学性质的最小粒子是分子,保持氨气的化学性质的最小粒子是氨分子;氨分子能使“铁树”上浸有无色酚酞试液的棉团由白色变成红色;故答案为:红;B;
(2)二氧化碳气体能和浓氢氧化钙溶液迅速反应,装置内气压减小,外界大气压将熟鸡蛋“吞”入瓶中,反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O;
故填:Ca(OH)2+CO2=CaCO3↓+H2O;
(3)白磷能在水下燃烧,其实质是白磷和氧气反应生成了五氧化二磷,其化学方程式为:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;白磷在热水下,没通氧气前不能燃烧,通入氧气后能燃烧,说明燃烧需要与氧气接触;在热水中能燃烧说明燃烧需要达到燃烧所需要的最低温度即物质的着火点;故答案为:最低温度;与氧气接触;4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;(4)二氧化碳能与水反应生成碳酸,碳酸能使石蕊变红,反应的方程式是:H2O+CO2═H2CO3.故填:二氧化碳能与水反应生成碳酸,碳酸能使石蕊变红;CO2+H2O=H2CO3;
【综合应用】【综合应用】该反应放出的热量使钾的温度达到钾物质的着火点;根据质量守恒定律及碱类物质的由金属与氢氧根组成的特点,可判断钾与水反应生成的碱为氢氧化钾,同时放出氢气;
故答案为:放热;2K+2H2O═2KOH+H2↑.
点评 本题主要考查酸碱指示剂与酸碱显示不同的颜色及二氧化碳、白磷的性质,还涉及到燃烧的条件使用,此题为基础性题型,但需学生活用所学知识.

| A. | 单宁酸由碳、氢、氧三种元素组成 | |
| B. | 1个单宁酸分子由76个碳原子、52个氢原子和46个氧原子构成 | |
| C. | 单宁酸分子中碳、氢、氧原子个数比为38:26:23 | |
| D. | 1个单宁酸分子中含有23个氢分子 |
| A. | CO、CO2、H2、O2 | B. | CO2、CO、O2、H2 | C. | H2、O2、CO2、CO | D. | CO、O2、H2、CO2 |
| A.性质与用途 | B.生活常识 |
| 铜具有导电性---制造炮弹 干冰易升华---作致冷剂 石蕊遇酸碱变色---作酸碱指示剂 | 鉴别羊毛纤维---点燃嗅闻有烧毛发味 新装修居室---一定挥发出有毒气体 人类可利用的氢气---为三大化石燃料之一 |
| C.化学之最 | D.初中化学的“三” |
| 最简单的有机物---氢气 最轻的气体---甲烷 最早湿法炼铜的国家---中国 | 单质可分为三类---金属、非金属、稀有气体 有还原性的三种物质---氢气、一氧化碳、炭 农作物肥料“三要素”---氮、磷、钾 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 除氢氧化钠溶液中的硫酸钠,加入适量氢氧化钡溶液后过滤 | |
| B. | 利用过滤方法分离硝酸钾与氯化钠 | |
| C. | 通过灼热的氧化铜方法除去二氧化碳中混有的少量一氧化碳 | |
| D. | 除去一氧化碳中混有的少量二氧化碳通入氢氧化钠溶液 |
| A. | CO2 | B. | H2O | C. | CO | D. | N2 |