题目内容
中国登山协会为纪念我国攀登珠穆朗玛峰成功50周年,再次组织攀登珠峰活动.阿旺扎西等一行登山运动员于2003年5月21日成功登顶.假如每位运动员冲顶时消耗自带的液氧4.8kg.求:
(1)这些氧气在标准状况下的体积是多少升?(标准状况下氧气的密度为1.43g/L)
(2)若在实验室用高锰酸钾为原料制取相同质量氮的氧气,需要多少kg的高锰酸钾?
(3)用这种方法给登山运动员供氧,是否可行?简述理由.
(1)这些氧气在标准状况下的体积是多少升?(标准状况下氧气的密度为1.43g/L)
(2)若在实验室用高锰酸钾为原料制取相同质量氮的氧气,需要多少kg的高锰酸钾?
(3)用这种方法给登山运动员供氧,是否可行?简述理由.
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:(1)根据氧气的质量、密度可以计算一定质量的氧气的体积;
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,根据氧气的质量可以计算高锰酸钾的质量;
(3)根据反应条件可以判断某种供氧方法说法可行.
(2)高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,根据氧气的质量可以计算高锰酸钾的质量;
(3)根据反应条件可以判断某种供氧方法说法可行.
解答:解:(1)4.8kg氧气在标准状况下的体积为:4800g÷1.43g/L=3356.64L,
答:4.8kg氧气在标准状况下的体积为3356.64L.
(2)设需要高锰酸钾的质量为x,
2KMnO4
K2MnO4+MnO2+O2↑,
316 32
x 4.8kg
=
,
x=47.4kg,
答:需要高锰酸钾的质量为47.4kg.
(3)因为利用高锰酸钾制取氧气需要加热,进而需要很多设备,既不利于简单、快速的制取氧气,又增加了负重,所以用这种方法给登山运动员供氧是不可行的.
答:4.8kg氧气在标准状况下的体积为3356.64L.
(2)设需要高锰酸钾的质量为x,
2KMnO4
| ||
316 32
x 4.8kg
| 316 |
| x |
| 32 |
| 4.8kg |
x=47.4kg,
答:需要高锰酸钾的质量为47.4kg.
(3)因为利用高锰酸钾制取氧气需要加热,进而需要很多设备,既不利于简单、快速的制取氧气,又增加了负重,所以用这种方法给登山运动员供氧是不可行的.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
相关题目
下列说法正确的是( )
| A、点燃可燃性气体时,都要先检验气体纯度 |
| B、用加氧气点燃的方法除去二氧化碳中混有的少量一氧化碳 |
| C、用燃着的木条鉴别氮气和二氧化碳 |
| D、用带火星的木条可以鉴别空气和二氧化碳 |
下列关于O2和CO2的“自述”中,属于物理性质的是( )
A、 |
B、 |
C、 |
D、 |
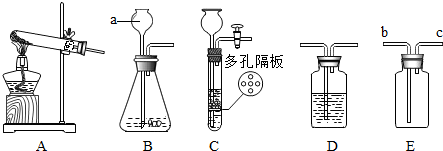 请结合下列实验常用装置,回答有关问题.
请结合下列实验常用装置,回答有关问题. 金属材料在生活、生产中应用十分广泛.
金属材料在生活、生产中应用十分广泛. 如图有多种功能,如收集气体、洗涤气体、贮存气体等,回答下列问题:
如图有多种功能,如收集气体、洗涤气体、贮存气体等,回答下列问题: