题目内容
20.Na2SO4、Na2SO3、Na2S三种物质组成的混合物中,测得钠元素的质量分数为23%,则其中氧元素的质量分数为61%.分析 根据所给物质的化学式进行分析,可以发现,在这三种物质中,钠元素与硫元素的原子个数比为2:1,也就是钠元素和硫元素的质量比是定值,从而确定氧元素的质量分数.
解答 解:在这三种物质中,钠元素与硫元素的原子个数比为2:1,也就是钠元素和硫元素的质量比是定值:$\frac{46}{32}$,所以若钠元素的质量分数是23%,则硫元素的质量分数为16%,故氧元素的质量分数为:1-23%-16%=61%.
故答案为:61%.
点评 本题考查了混合物中某元素质量分数的求算,完成此题,可以依据物质中元素的固定质量比进行.

练习册系列答案
 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案
相关题目
10.某固体可能含有Ca(NO3)2、Na2SO4、Na2CO3、FeCl3、KCl中的一种或几种,现对其进行如下实验:①取少量固体于试管中,加适量蒸馏水,固体完全溶解成无色透明溶液②取少量上述溶液,加过量稀硝酸,有气泡产生;③取②所得溶液少量,滴加BaCl2溶液,产生白色沉淀.分析以上实验现象,对原固体组成的推断中正确的是( )
| A. | 肯定有Na2CO3,Na2SO4,无FeCl3、Ca(NO3)2 | |
| B. | 肯定有Na2CO3,无FeCl3、Ca(NO3)2 | |
| C. | 肯定有Na2CO3,Na2SO4,无FeCl3 | |
| D. | 肯定有Na2CO3,无FeCl3,KCl |
11.下列净化水的方法中属于化学方法的是( )
| A. | 消毒剂杀菌 | B. | 自然沉降 | C. | 过滤 | D. | 活性炭吸附 |
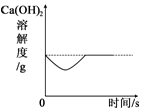
8.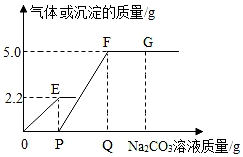 向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液,反过应程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法正确的是( )
向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液,反过应程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法正确的是( )
 向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液,反过应程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法正确的是( )
向一定量CaCl2和HCl的混合溶液中,逐渐加入Na2CO3溶液,反过应程中产生气体或沉淀的质量与加入的Na2CO3溶液的质量关系如图,下列说法正确的是( )| A. | 该反应先有沉淀后有气体,故不遵循质量守恒定律 | |
| B. | PF段有沉淀生成,溶液的PH保持不变约为7 | |
| C. | F点处溶液中的溶质有氯化钠、碳酸钠 | |
| D. | OE发生化学反应:Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
5.指出下列变化中哪一个属于分解反应( )
| A. | 氢气在空气中燃烧 | |
| B. | 过滤泥水得到水和泥沙 | |
| C. | 工业上用分离液态空气的方法获得氧气 | |
| D. | 铜绿加热后变黑 |
9. 国庆小长假,某校学生佳明同学和小伙伴一起到革命老区参观游览,接受革命传统教育,请你用学过的化学知识解决他们在游览中遇到的问题:
国庆小长假,某校学生佳明同学和小伙伴一起到革命老区参观游览,接受革命传统教育,请你用学过的化学知识解决他们在游览中遇到的问题:
(1)他们进入景区大门,场地上各种鲜花盛开,香气扑鼻,用分子观点解释闻到花香的原因分子在不断的运动.
(2)他们在山顶进行了简单的午餐,下面的食品主要补充维生素的是C
A.面包 B.香肠 C.苹果 D.高钙牛奶
(3)返回下山途中,佳明拾取了一些不文明游客乱扔的物品,其中属于金属材料的是B
A.矿泉水瓶 B.易拉罐 C.塑料袋 D.门票及导游图
(4)佳明用空瓶装了一瓶山泉水带回实验室,对该山泉水进行净化提纯,其净化程度最高的方法是B(填序号)
A.过滤 B.蒸馏 C.沉淀 D.吸附.
(5)佳明了解到他们乘坐的飞机大量使用金属材料(图一),铝的金属活动性比铁的强(填“强”或“弱”)空气中,铝比铁具有更好的抗腐蚀性,原因是4Al+3O2=2Al2O3(用化学方程式解释)
(6)佳明在爬山途中休息时拿出自带的月饼与朋友分享,他发现包装袋内有一个装有活性炭铁粉脱氧保鲜剂(也称脱氧剂)的塑料小包,旅游回来后,佳明同学对脱氧剂进行了探究(图二):
①仔细观察,发现脱氧剂塑料包上有许多小孔,佳明认为这些小孔的作用可能是利于活性铁粉与氧气、水分接触;
②挤捏塑料包质感较硬,剪开塑料包将里面的脱氧剂倒在纸上,脱氧剂呈红褐色并已结块,佳明得出活性铁粉已部分被氧化的结论,由此推断,食品包装袋中放入脱氧剂的目的是除去包装袋内的氧气;
③为弄清上述脱氧剂有哪些成分,佳明将其带进实验室,继续探究:
 国庆小长假,某校学生佳明同学和小伙伴一起到革命老区参观游览,接受革命传统教育,请你用学过的化学知识解决他们在游览中遇到的问题:
国庆小长假,某校学生佳明同学和小伙伴一起到革命老区参观游览,接受革命传统教育,请你用学过的化学知识解决他们在游览中遇到的问题:(1)他们进入景区大门,场地上各种鲜花盛开,香气扑鼻,用分子观点解释闻到花香的原因分子在不断的运动.
(2)他们在山顶进行了简单的午餐,下面的食品主要补充维生素的是C
A.面包 B.香肠 C.苹果 D.高钙牛奶
(3)返回下山途中,佳明拾取了一些不文明游客乱扔的物品,其中属于金属材料的是B
A.矿泉水瓶 B.易拉罐 C.塑料袋 D.门票及导游图
(4)佳明用空瓶装了一瓶山泉水带回实验室,对该山泉水进行净化提纯,其净化程度最高的方法是B(填序号)
A.过滤 B.蒸馏 C.沉淀 D.吸附.
(5)佳明了解到他们乘坐的飞机大量使用金属材料(图一),铝的金属活动性比铁的强(填“强”或“弱”)空气中,铝比铁具有更好的抗腐蚀性,原因是4Al+3O2=2Al2O3(用化学方程式解释)
(6)佳明在爬山途中休息时拿出自带的月饼与朋友分享,他发现包装袋内有一个装有活性炭铁粉脱氧保鲜剂(也称脱氧剂)的塑料小包,旅游回来后,佳明同学对脱氧剂进行了探究(图二):
①仔细观察,发现脱氧剂塑料包上有许多小孔,佳明认为这些小孔的作用可能是利于活性铁粉与氧气、水分接触;
②挤捏塑料包质感较硬,剪开塑料包将里面的脱氧剂倒在纸上,脱氧剂呈红褐色并已结块,佳明得出活性铁粉已部分被氧化的结论,由此推断,食品包装袋中放入脱氧剂的目的是除去包装袋内的氧气;
③为弄清上述脱氧剂有哪些成分,佳明将其带进实验室,继续探究:
| 实验内容及现象 | 实验结论 | 反应的化学反应方程式 |
| 取部分红褐色并已结块的脱氧剂放入试管中,倒入足量稀盐酸,随脱氧剂的溶解,溶液变黄,溶液中有气泡产生 | 已结块的脱氧剂中含有铁粉与氧化铁 | Fe2O3+6HCl═2FeCl3+3H2O、Fe+2HCl=FeCl2+H2↑ |
10.对比法是学习化学的重要研究方法.下列实验方案设计中未采用对比法的是( )
| A. | 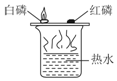 探究燃烧的条件 | B. | 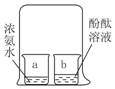 探究分子的性质 | ||
| C. | 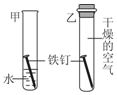 探究铁生锈的条件 | D. |  探究MnO2的催化作用 |