题目内容
3. 甲、乙两种固体的溶解度曲线如图所示.下列说法中,不正确的是( )
甲、乙两种固体的溶解度曲线如图所示.下列说法中,不正确的是( )| A. | 40℃时,甲的饱和瑢液中溶质和溶剂的质量比为1:2 | |
| B. | 乙的饱和溶液从40℃降到20℃时,溶液仍饱和 | |
| C. | 20℃时,甲、乙两溶液的溶质质量分数一定相等 | |
| D. | 20℃时,分别向l00g水中加入40g甲、乙,加热到40℃时,乙溶液为饱和溶液 |
分析 A、据该温度下甲的溶解度分析解答;
B、据乙的溶解度随温度降低而减小分析解答;
C、不知溶液中溶质、溶剂的质量,溶液的状态,无法判断溶质的质量分数大小;
D、据乙在不同温度下的溶解度分析解答.
解答 解:A、40℃时,甲物质的溶解度是50g,即100g水中最多溶解50g的甲,同一温度下物质的饱和溶液其组成相同,则饱和溶液中溶质和溶剂的质量比=50g:100g=1:2,正确;
B、乙的溶解度随温度降低而减小,所以其饱和溶液从40℃降到20℃时,析出晶体,溶液仍饱和,正确;
C、由甲、乙两种固体物质的溶解度曲线可知,20℃时,甲、乙的溶解度曲线交于一点,此温度时,甲、乙的溶解度相同,此时两种物质饱和溶液的溶质质量分数也相同的.若不是饱和溶液,不能比较.故错误;
D、20℃时二者的溶解度相等,是30g,所以分别向l00g水中加入40g甲、乙,均不能完全溶解,最多溶解30g,加热到40℃时,乙的溶解度变为40g,恰好为饱和溶液,正确;
故选:C.
点评 通过回答本题知道了溶解度曲线表示的意义,饱和溶液溶质质量分数与溶解度的关系等知识,并能结合题意灵活解答.

练习册系列答案
相关题目
14.咱们学校化学兴趣小组的同学,对实验室制备氧气的若干问题进行如下探究:
【探究一】为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
(1)写出本实验中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;测量O2体积的装置是c (选填下图l中的装置编号).

(2)由实验I、II、III可知:影响双氧水分解速率的因素是:双氧水的浓度.
【探究二】B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.于是他们用天平称量0.2g氧化铜,取5%过氧化氢溶液5mL于试管中,进行如图2实验:

(1)填写如表:
(2)步骤①的目的是与步骤③对比,检验加入氧化铜前后过氧化氢溶液的分解速率有无变化,步骤④对应的实验操作是过滤,步骤⑦是证明氧化铜的化学性质在反应前后没有改变.
【探究一】为探究影响双氧水分解速率的某种因素,A小组记录了如下实验数据:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2的体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |

(2)由实验I、II、III可知:影响双氧水分解速率的因素是:双氧水的浓度.
【探究二】B小组查阅资料:在过氧化氢溶液的分解反应中,氧化铜也能作催化剂.于是他们用天平称量0.2g氧化铜,取5%过氧化氢溶液5mL于试管中,进行如图2实验:

(1)填写如表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦操作 | 结论 |
| 有大量气泡产生. | 称得氧化铜质量为0.2g. | 将固体加入盛有5mL 5%过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象. | 在过氧化氢溶液的分解实验中,氧化铜也能作催化剂. |
11.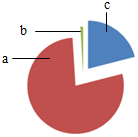 如图为空气成分示意图(按体积计算),其中“a”代表的是( )
如图为空气成分示意图(按体积计算),其中“a”代表的是( )
 如图为空气成分示意图(按体积计算),其中“a”代表的是( )
如图为空气成分示意图(按体积计算),其中“a”代表的是( )| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 稀有气体 |
18. 如图是电解水的实验装置.下列说法中,正确的是( )
如图是电解水的实验装置.下列说法中,正确的是( )
 如图是电解水的实验装置.下列说法中,正确的是( )
如图是电解水的实验装置.下列说法中,正确的是( )| A. | 电解水的方程式为2H2O=H2↑+O2↑ | |
| B. | 实验说明水是甶氢原子和氧原子构成的 | |
| C. | 2管内产生的气体能使木条复燃 | |
| D. | 1、2两试管产生的气体质量之比为2:1 |
13.物质的用途和性质密切相关.下列说法错误的是( )
| A. | 氧气用于医疗急救--氧气能提供呼吸 | |
| B. | 氮气用于食品防腐包装--氮气的化学性质不活泼 | |
| C. | 稀有气体充入霓虹灯--稀有气体充电能发出不同颜色的光 | |
| D. | 氧气用于气焊--氧气具有可燃性 |
 根如图回答问题.
根如图回答问题.