题目内容
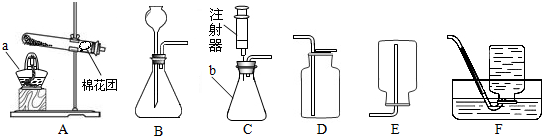
 如图是镁、锌、铁、铜四种金属与稀盐酸反应的示意图:
如图是镁、锌、铁、铜四种金属与稀盐酸反应的示意图:(1)根据图中现象分析,A表示的金属是
(2)根据图中现象可知,四种金属中活动性最强弱的是
(3)写出金属C与盐酸反应的化学方程式
(4)由图中现象可知,影响金属与酸反应快慢的因素有
考点:金属的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:在金属活动性顺序中,只有排在氢前的金属才可以和稀酸溶液反应生成氢气,而且越靠前的金属活动性就越强,和稀酸溶液反应时现象就越剧烈,根据这一规律可以判断反应的发生或者验证金属的活动性强弱.
解答:解:(1)四种金属中,镁的活动性最强,与稀盐酸反应最剧烈,故A表示的金属是镁;
(2)所以从图中可以看出,镁反应最剧烈,其次是锌,然后是铁,不反应的为铜,四种金属中活动性最强弱的是铜
(3)金属C应是金属铁,与盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑;
(4)由图可见金属的种类(或性质)不同,与酸反应快慢不同.
故答案为:(1)镁;(2)铜;(3)Fe+2HCl═FeCl2+H2↑;
(4)金属的种类(或性质)
(2)所以从图中可以看出,镁反应最剧烈,其次是锌,然后是铁,不反应的为铜,四种金属中活动性最强弱的是铜
(3)金属C应是金属铁,与盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑;
(4)由图可见金属的种类(或性质)不同,与酸反应快慢不同.
故答案为:(1)镁;(2)铜;(3)Fe+2HCl═FeCl2+H2↑;
(4)金属的种类(或性质)
点评:本题难度不是很大,主要考查了对金属活动性顺序的应用,从而培养学生对金属活动性顺序的理解和应用.

练习册系列答案
相关题目
下列现象中,不是化学变化引起的是( )
| A、古建筑中石像变模糊 |
| B、地下煤层自燃 |
| C、溶洞的形成 |
| D、分离液态空气制氧气 |
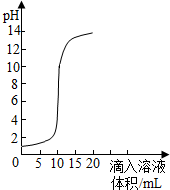 (1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成
(1)向盛有氢氧化钠溶液的锥形瓶里滴入几滴酚酞溶液,溶液变成