��Ŀ����
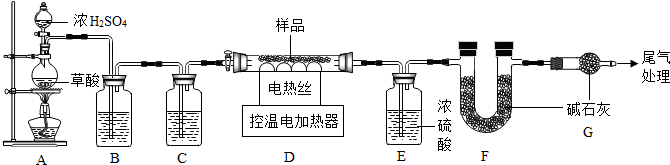
15���������ʵ��װ��ͼ���ش�ͼ������⣺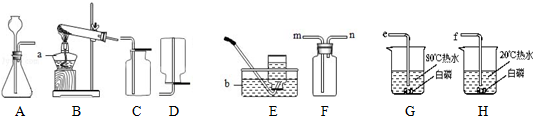
��1������A��F��ʾ��ʵ������ȡ����ʱ���õ�װ�ã��ش��������⣺
��д��ͼ���б�ŵ��������ƣ�a���ƾ���
����A��Bװ�ö�������ȡ��������Bװ�ü��ȸ��������ȡ����ʱ���Թܿڻ�Ҫ��һ������Ŀ���Ƿ�ֹ��ĩ�����Թܣ�C��E��F���������ռ�����������Eװ���ռ�������ԭ����������������ˮ������Fװ���ռ�����������Ӧ��m�˽��루�m����n������
��2���������������ֱ�ͨ��G��Hװ���У��۲쵽G��H�е�����ͬ����һ��ʵ˵����ȼ��ȼ�ձر��������DZ���ﵽ��ȼ����Ż�㣮
���� ��1��������������ƣ���ȷʵ���е�ע�������Լ��ռ������ķ�����
��2�����ݿ�ȼ��ȼ�յ�������������
��� �⣺��1��������a�Ǿƾ��ƣ�����ƾ��ƣ�
�ڼ��ȸ��������ȡ����ʱ����Ҫ���Թܿڴ�����һ���ţ��Է�������ؿ������뵼���ܣ���Ϊ������������ˮ�����Կ�����ˮ�����ռ����������ܶȱȿ�����������Eװ�����ռ�ʱ������ӳ��ܽ��룻���������ֹ��ĩ�����Թܣ�������������ˮ��m��
��2��G�еİ���ȼ�գ�H�еİ���û��ȼ�գ�˵���˿�ȼ��ȼ���¶ȱ���ﵽ���Ż�㣻�������ﵽ��ȼ����Ż�㣮
���� ����Ƚϼ���Ҫ������ʵ������ȡ���巢��װ�õ�ѡȡ���ռ�װ�õ�ѡ�Ȿ��Ĺؼ���Ҫ��������ʵ�������ѡ������װ�ã�

��ϰ��ϵ�д�
 ����С״Ԫ��������������ϵ�д�
����С״Ԫ��������������ϵ�д�
�����Ŀ
5��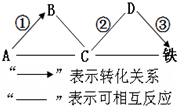 A��B��C��D�ֱ�Ϊ�����������ᡢ�������ơ�̼����е�һ�֣�����֮��ķ�Ӧ��ת����ϵ��ͼ���������ʺͷ�Ӧ��������ȥ��������˵������ȷ���ǣ�������
A��B��C��D�ֱ�Ϊ�����������ᡢ�������ơ�̼����е�һ�֣�����֮��ķ�Ӧ��ת����ϵ��ͼ���������ʺͷ�Ӧ��������ȥ��������˵������ȷ���ǣ�������
 A��B��C��D�ֱ�Ϊ�����������ᡢ�������ơ�̼����е�һ�֣�����֮��ķ�Ӧ��ת����ϵ��ͼ���������ʺͷ�Ӧ��������ȥ��������˵������ȷ���ǣ�������
A��B��C��D�ֱ�Ϊ�����������ᡢ�������ơ�̼����е�һ�֣�����֮��ķ�Ӧ��ת����ϵ��ͼ���������ʺͷ�Ӧ��������ȥ��������˵������ȷ���ǣ�������| A�� | C���������� | |
| B�� | ��Ӧ�ٵĻ�ѧ����ʽ�����ǣ�CO2+Ca��OH��2�TCaCO3��+H2O | |
| C�� | ��Ӧ����������Һ��dz��ɫ | |
| D�� | ��Ӧ����D���ʿɷ�����ԭ��Ӧ�õ��� |
10������һ����;�㷺����Ҫ�Ļ���ԭ�ϣ�����Ӳ��Ӳ�Ƚ����ڽ��ʯ��������������������þ��Ӧ��ȡ���ʣ��䷴Ӧ�Ļ�ѧ����ʽΪB2O3+3Mg$\frac{\underline{\;ȼ��\;}}{\;}$3MgO+mB��������˵����ȷ���ǣ�������
| A�� | �û�ѧ����ʽ��m=2 | B�� | �÷�Ӧ��ֻ�漰һ�������� | ||
| C�� | �÷�Ӧ���ڻ��Ϸ�Ӧ | D�� | �÷�Ӧ��ԭ�ӵ�������˱仯 |
20���������ڻ�ѧ�仯���ǣ�������
| A�� | ʳ������ | B�� | ��ˮɹ�� | C�� | ����ȼ�� | D�� | �ɱ����� |
7�����г��ӵķ�����ȷ���ǣ�������
| ѡ�� | ���� | ���� | �����ʵķ��� |
| A | CaO | CaCO3 | ��ˮ������ |
| B | K2CO3��Һ | KCl | ������ϡ���ᣬ���� |
| C | CaCl2��Һ | ϡ���� | �ӹ���̼��ƣ����� |
| D | NaCl��Һ | Na2CO3 | �������������Һ������ |
| A�� | A | B�� | B | C�� | C | D�� | D |
4�������������
��������
| ѡ�� | ���� | ���ʻ��� |
| A | ����ϳɲ��� | ���ϡ��ϳ����ϳ���ά |
| B | ����ʯȼ�� | ú��ʯ�͡���Ȼ�� |
| C | �������ʵ������� | ���ӡ�ԭ�ӡ����� |
| D | ͬһ���ʵ��������� | ���ռ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |