题目内容
17.写出下列微粒的化学符号:①银原子Ag; ②氨气分子NH3;
③硫酸根离子SO42-; ④人体中含量最多的元素O.
分析 (1)原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字.
(2)分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字.
(3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.
(4)人体中含量最多的元素是氧元素,写出其元素符号即可.
解答 解:(1)由原子的表示方法,用元素符号来表示一个原子,表示多个该原子,就在其元素符号前加上相应的数字,故银原子表示为:Ag.
(2)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字,则氨分子可表示为:NH3.
(3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.硫酸根离子可表示为:SO42-.
(4)人体中含量最多的元素是氧元素,其元素符号为:O.
故答案为:(1)Ag;(2)NH3;(3)SO42-;(4)O.
点评 本题难度不大,掌握常见化学用语(元素符号、原子符号、分子符号、离子符号等)的书写方法、离子符号与化合价表示方法的区别等是正确解答此类题的关键.

练习册系列答案
 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案
相关题目
5.下列混合气体点燃可能发生爆炸的是( )
| A. | 氮气和氧气 | B. | 一氧化碳和二氧化碳 | ||
| C. | 天然气和空气 | D. | 氦气和氧气 |
2.菱镁矿的主要成分是MgCO3,为了分析某菱镁矿中镁元素的含量,某班学习小组进行了实验探究,取10g菱镁矿样品,逐渐加入未知浓度的H2SO4溶液,生成的气体全部用NaOH溶液吸收,NaOH溶液增加的质量记录如表:
注:菱镁矿中的杂质不溶于水,不与酸发生反应、不含镁元素.请回答:
(1)10g菱镁矿与稀硫酸完全反应,生成气体的质量为4.4g.
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)吸收反应生成的气体,不用石灰水的原因是氢氧化钙的溶解度常温下很小,所以等质量的石灰水和氢氧化钠溶液中,氢氧化钠溶液的质量分数更大,可吸收更多的二氧化碳.
| 分组 | 1 | 2 | 3 | 4 |
| 加入H2SO4溶液质量/g | 50 | 100 | 150 | 200 |
| NaOH溶液增加质量/g | 2.2 | 4.4 | 4.4 | 4.4 |
(1)10g菱镁矿与稀硫酸完全反应,生成气体的质量为4.4g.
(2)计算该菱镁矿中镁元素的质量分数.(写出计算过程)
(3)吸收反应生成的气体,不用石灰水的原因是氢氧化钙的溶解度常温下很小,所以等质量的石灰水和氢氧化钠溶液中,氢氧化钠溶液的质量分数更大,可吸收更多的二氧化碳.
9.下列各组物质中按酸、碱、盐、氧化物的顺序排列的是( )
| A. | H2SO4、Na2O、MgCl2、CO | B. | NaHCO3、Ba(OH)2、NaCl、O2 | ||
| C. | HNO3、KOH、Na2CO3、MnO2 | D. | HCl、NaOH、K2CO3、KMnO4 |
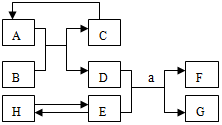 已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能使澄清石灰水变浑浊;B为红棕色固体,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答:
已知A-H均为初中化学常见的物质.其中A、C是组成元素相同的气体,且C能使澄清石灰水变浑浊;B为红棕色固体,是赤铁矿的主要成分;F是紫红色金属;H是蓝色沉淀.根据如图所示的转化关系(图中反应条件均已略去),请回答: 某同学为了探究物质的性质,以氧气为例,做了如下实验:如图所示.先收集了两瓶氧气(注意:瓶口向上)后正放在桌上,盖好玻璃片,然后用带火星的木条插入A集气瓶中,在B瓶中放入一只昆虫.请回答下列问题:
某同学为了探究物质的性质,以氧气为例,做了如下实验:如图所示.先收集了两瓶氧气(注意:瓶口向上)后正放在桌上,盖好玻璃片,然后用带火星的木条插入A集气瓶中,在B瓶中放入一只昆虫.请回答下列问题: