题目内容
13.为了测定某含杂质7%的黄铜样品中铜的质量分数(黄铜主要成分为铜和锌,并含有少量杂质.杂质中不含铜、锌元素,杂质不溶于水,不与其它物质反应,受热也不分解),某化学小组进行了如下实验: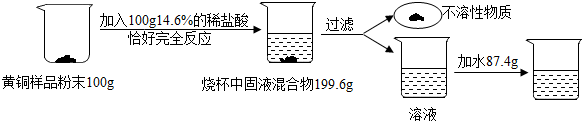
(1)该黄铜样品中铜的质量分数是多少?
(2)向过滤后所得滤液中加入87.4g水,则最终所得溶液之中溶质的质量分数是多少?
分析 (1)根据质量守恒定律可以计算出反应生成氢气的质量,然后结合反应的化学方程式可以得出求锌的质量比例式;根据锌与杂质的质量分析铜的质量;
(2)反应后的溶液为氯化锌溶液,根据化学方程式结合溶液中溶质的质量分数的计算公式可以完成解答;
解答 解:(1)反应生成氢气的质量为:100g+100g-199.6g=0.4g
设合金中锌的质量为X,反应生成氯化锌的质量为y
Zn+2HCl═ZnCl2+H2↑
65 136 2
X y 0.4g
$\frac{65}{x}=\frac{136}{y}=\frac{2}{0.4g}$
解得:X=13g
y=27.2g
该黄铜样品中铜的质量分数是$\frac{100g-13g-100g×7%}{100g}$×100%=80%
(2)最终所得溶液中溶质的质量分数为:$\frac{27.2g}{13g+100g+87.4g-0.4g}$×100%=13.6%
故答案为:(1)80%;
(2)13.6%.
点评 本题主要考查了根据化学方程式的计算,要想解答好这类题目,就要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的物质的质量等知识.

练习册系列答案
相关题目
3.某实验小组想测定黄铜中铜的质量分数,实验数据记录如下:
(1)根据实验数据分析,从实验4开始金属已经完全反应.
(2)计算黄铜中铜的质量分数.(精确到0.1%)
(3)计算所用稀硫酸的溶质质量分数.(精确到0.1%)
| 样品 | 实验1 | 实验2 | 实验3 | 实验4 | 实验5 |
| 黄铜质量\g | 40 | 40 | 40 | 40 | 40 |
| 加入稀硫酸质量\g | 30 | 60 | 90 | 120 | 150 |
| 生成气体质量\g | 0.3 | 0.6 | 0.9 | 1.0 | 1.0 |
(2)计算黄铜中铜的质量分数.(精确到0.1%)
(3)计算所用稀硫酸的溶质质量分数.(精确到0.1%)
4.下列物质中含有氧分子的是( )
| A. | 二氧化碳 | B. | 空气 | C. | 过氧化氢 | D. | 水 |
1.从微观角度分析,下列解释错误的是( )
| A. | 液氧和氧气都能助燃--同种分子化学性质相同 | |
| B. | 吹胀气球--气体分子体积变大 | |
| C. | 缉毒犬能根据气球发现毒品--分子在不断运动 | |
| D. | 水电解生成氢气和氧气--化学变化中,分子变成原子,原子重新结合成分子 |
18.同学们在学习碱的化学性质时,进行了如图所示的实验.
(1)写出甲实验中盐酸和氢氧化钠反应的化学方程式NaOH+HCl═NaCl+H2O.
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是气球胀大.
(3)丙实验中观察到试管内有白色沉淀产生.
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问.

(1)写出甲实验中盐酸和氢氧化钠反应的化学方程式NaOH+HCl═NaCl+H2O.
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是气球胀大
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、水和氯化钠(写物质名称).
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有
如下猜想.
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是氢氧化钠.(写一种猜想)
【实验设计】小方想用氯化钙溶液来验证小云、小红、小林的猜想.查阅资料获悉氯化钙溶液呈中性,并设计如下实验.请你将小方的实验设计补充完整.
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑反应物是否有剩余.
(1)写出甲实验中盐酸和氢氧化钠反应的化学方程式NaOH+HCl═NaCl+H2O.
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是气球胀大.
(3)丙实验中观察到试管内有白色沉淀产生.
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色,产生疑问.

(1)写出甲实验中盐酸和氢氧化钠反应的化学方程式NaOH+HCl═NaCl+H2O.
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是气球胀大
【提出问题】废液中含有哪些物质?
【交流讨论】①一定含有的物质:碳酸钙、指示剂、水和氯化钠(写物质名称).
②还含有能使废液呈碱性的物质.能使废液呈碱性的物质是什么?同学们有
如下猜想.
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
你认为还可能是氢氧化钠.(写一种猜想)
| 实验内容 | 预计现象 | 预计结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置. | ①有白色沉淀,溶液呈红色. | 小林的猜想正确. |
| ②无现象,溶液呈红色. | 小红的猜想正确. | |
| ③有白色沉淀,溶液呈无色. | 小云的猜想正确. |
【反思拓展】在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑反应物是否有剩余.
5.下列物质为纯净物的是( )
| A. | 农夫山泉有点甜 | B. | 双宝钙质鲜牛奶 | C. | 液氧 | D. | 雪花啤酒 |
2. 根据A物质和B物质的溶解度曲线,回答下列问题:
根据A物质和B物质的溶解度曲线,回答下列问题:
(1)40℃时,将50gA物质和50gB物质分别放入盛有100g水的烧杯里,充分搅拌,烧杯中的溶液没有达到饱和的是A物质,该溶液的溶质质量分数是33.3%(保留1位小数).
(2)将题(1)所述溶液从40℃降温至30℃,两烧杯中均析出一些固体.析出的A物质和B物质的质量关系是A物质=B物质(填>、<、=).
(3)C物质的溶解度如下表,请在图中描出C物质的溶解度曲线.
 根据A物质和B物质的溶解度曲线,回答下列问题:
根据A物质和B物质的溶解度曲线,回答下列问题:(1)40℃时,将50gA物质和50gB物质分别放入盛有100g水的烧杯里,充分搅拌,烧杯中的溶液没有达到饱和的是A物质,该溶液的溶质质量分数是33.3%(保留1位小数).
(2)将题(1)所述溶液从40℃降温至30℃,两烧杯中均析出一些固体.析出的A物质和B物质的质量关系是A物质=B物质(填>、<、=).
(3)C物质的溶解度如下表,请在图中描出C物质的溶解度曲线.
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 40 | 33 | 27 | 23 | 18 | 14 | 10 |
3.下列说法正确的是( )
| A. | H2SO4、NaCl、NaOH三者溶液的pH逐渐变小 | |
| B. | 黄铜的硬度比纯铜大 | |
| C. | 同温等质量的KNO3、NaCl、CaO固体三者放入100g水中后,所得溶液的浓度逐渐降低 | |
| D. | K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高 |