题目内容
9.常温下,A、B均为液态,且组成元素相同;D溶液常用来检验二氧化碳气体的存在,Y为氧化物,Z是紫红色固体.各物质间的转化关系如图所示(个别产物略去)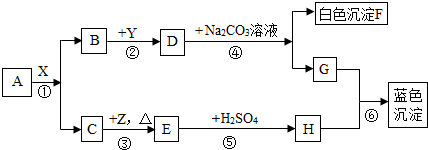
(1)推断:A是H2O2,E是CuO.(写化学式)
(2)反应④结束后,从混合物中分离出F的操作是过滤;农业上常用H 和石灰加水配制杀虫剂波尔多液,波尔多液不能用铁制容器盛放的原因是Fe+CuSO4=FeSO4+Cu(用化学方程式解释)
(3)写出化学方程式④Ca(OH)2+Na2CO3=2NaOH+CaCO3↓.
(4)写出化学方程式⑤CuO+H2SO4=CuSO4+H2O.
分析 (1)D和碳酸钠反应生成白色沉淀F,D溶液常用来检验二氧化碳气体的存在,D就是氢氧化钙,所以F就是碳酸钙,而Y为氧化物,所以Y就是氧化钙,B就是水,G就是氢氧化钠,E和硫酸生成H,说明H中有硫酸根离子,我们所接触的蓝色沉淀,应该是铜的沉淀,所以H是硫酸铜,A.B均为液态,且组成元素相同,并且又会生成水的,可以推出A就是双氧水,C就是氧气,所以E就是氧化铜,Z是紫红色固体金属铜.
(2)根据固液混合物的分离方法进行分析,根据金属活动性顺序和置换反应的原理分析;
(3)根据反应的原理进行分析;
(4)根据反应的原理进行分析.
解答 解:(1)D和碳酸钠反应生成白色沉淀F,D溶液常用来检验二氧化碳气体的存在,D就是氢氧化钙,所以F就是碳酸钙,而Y为氧化物,所以Y就是氧化钙,B就是水,G就是氢氧化钠,E和硫酸生成H,说明H中有硫酸根离子,我们所接触的蓝色沉淀,应该是铜的沉淀,所以H是硫酸铜,A.B均为液态,且组成元素相同,并且又会生成水的,可以推出A就是双氧水,C就是氧气,所以E就是氧化铜,Z是紫红色固体金属铜.
故答案为:H2O2,CuO;
(2)反应④结束后,产物为碳酸钙沉淀和氢氧化钠溶液,要将可溶物和不溶物进行分离,需要进行过滤,所以用过滤的方法从混合物中分离出F碳酸钙,故答案为:过滤;铁在金属活动顺序中排在铜之前,会将铜从硫酸铜中置换出来,反应的化学方程式是:Fe+CuSO4=FeSO4+Cu;故答案为:Fe+CuSO4=FeSO4+Cu;
(3)氢氧化钙和碳酸钠生成碳酸钙沉淀和氢氧化钠,故化学方程式④为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(4)氧化铜和硫酸反应生成硫酸铜和水,故化学方程式⑤为:CuO+H2SO4=CuSO4+H2O.
本题答案为:(1)H2O2,CuO;
(2)过滤;Fe+CuSO4=FeSO4+Cu;
(3)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;
(5)CuO+H2SO4=CuSO4+H2O.
点评 本题主要考查了对物质进行鉴别的方法,以及混合物的正确的分离方法.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 在两支试管中各装少许CuSO4溶液,分别加入锌片和铁片 | |
| B. | 在两支试管中各装少许FeSO4溶液,分别加入锌片和铜片 | |
| C. | 向盛稀盐酸的两支试管中,分别加入锌片和铁片,再向盛FeSO4溶液的试管中,加入铜片 | |
| D. | 向盛有ZnSO4溶液和CuSO4溶液的两支试管里分别加入铁片 |
| A. | 铁+硫酸-→硫酸亚铁+氢气 | B. | 氧气+一氧化碳二氧化碳 | ||
| C. | 氢气+氯气氯化氢 | D. | 氧化钙+水--→氢氧化钙 |
| A. | 燃起篝火烘烤食物 | B. | 太阳能热水器烧水 | ||
| C. | 绿色植物将太阳能转化为化学能 | D. | 煤燃烧发电 |
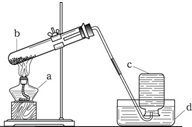 用高锰酸钾制取并收集氧气使用如图的装置,图中有三处错误,请指出其中的错误.
用高锰酸钾制取并收集氧气使用如图的装置,图中有三处错误,请指出其中的错误.