题目内容
2. 某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )
某电镀厂的电镀液中含有金盐,为了回收其中的金元素,技术人员制作了如图的“吸金球”,“吸金球”是装入一些“吸金”物质的纱袋,把“吸金球”浸入电镀液,能“吸”出盐溶液中的金,据上所述,“吸金球”中的“吸金”物质可能是( )| A. | 活性炭(C) | B. | 铁屑(Fe) | ||
| C. | 硫酸铜(CuSO4) | D. | 磁石(主要成分是Fe3O4) |
分析 根据在金属活动顺序表中,排在前边的金属可以把后边的金属从其盐溶液中置换出来结合选项的物质分析.
解答 解:A、碳和金盐不反应,故A错误;
B、铁的活动性比金强,可以和金盐发生置换反应,故B正确;
C、硫酸铜不能和金盐发生置换反应产生金,故C错误;
D、四氧化三铁和金盐不反应,故D错误.
故选:B.
点评 本题考查了金属的回收利用,依据金属活动性的顺序分析即可,要注意所加的物质能与金离子反应进行分析.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
15.小馨同学在复习化学知识时,有如下归纳或总结,你认为不正确的是( )
| A. | 碱都含有氢元素,但含有氢元素的化合物不一定是碱 | |
| B. | 糖类、蛋白质、油脂、纤维素、盐和水,通常称为营养素 | |
| C. | 用加水溶解的方法检验纯碱中是否混入了食盐 | |
| D. | 中和反应有盐和水生成,有盐和水生成的反应不一定是中和反应 |
7.某同学在实验室进行了木炭还原氧化铜的实验,实验步骤如下:
⑤为确定木炭还原氧化铜后的固体成分,请你与兴趣小组的同学完成以下探究(注:该反应还原产物只有铜).
【猜想】猜想Ⅰ:全部都是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、木炭.
【实验与结论】待试管冷却后将剩余固体倒入烧杯,加入足量稀硫酸,过滤,得到蓝色滤液,
滤渣为红色和黑色固体混合物.证明猜想猜想Ⅳ成立;写出氧化铜与稀硫酸反应的化学方程式CuO+H2SO4═CuSO4+H2O.
【实验反思】混合物中仍含有氧化铜的原因可能是碳和氧化铜没有完全反应就停止了加热,或者还可能的原因是从试管B中撤出导管时,有空气进入试管,与灼热的铜再次反应生成氧化铜.
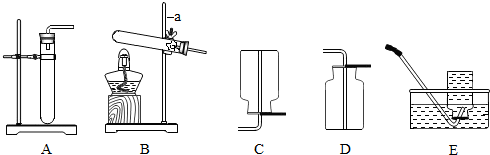
| 实验装置 | 实验步骤 | 分析 |
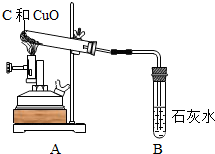 | ①检验装置气密性 | |
| ②把木炭和氧化铜的混合物放入试管,如左图所示连接实验装置 | 装置中存在的问题是B试管处不应该有橡皮塞 | |
| ③改进装置后,点燃酒精喷灯开始实验 | 装置B的作用是检验产物是否有二氧化碳 | |
| ④反应结束时,先将导管从装置B中撤出,再停止加热 | 目的是防止液体倒流引起试管炸裂 |
【猜想】猜想Ⅰ:全部都是金属铜; 猜想Ⅱ:除铜外,还含有氧化铜;
猜想Ⅲ:除铜外,还含有木炭; 猜想Ⅳ:除铜外,还含有氧化铜、木炭.
【实验与结论】待试管冷却后将剩余固体倒入烧杯,加入足量稀硫酸,过滤,得到蓝色滤液,
滤渣为红色和黑色固体混合物.证明猜想猜想Ⅳ成立;写出氧化铜与稀硫酸反应的化学方程式CuO+H2SO4═CuSO4+H2O.
【实验反思】混合物中仍含有氧化铜的原因可能是碳和氧化铜没有完全反应就停止了加热,或者还可能的原因是从试管B中撤出导管时,有空气进入试管,与灼热的铜再次反应生成氧化铜.