题目内容
1.现有氯酸钾和二氧化锰混合物12克,加热至不再产生气体后,冷却到室温,把试管内固体溶解在14.6克水中,结果有3.82克固体剩余,再继续加2克水,仍有3.18克固体未溶解.(1)若该3.18克固体都是二氧化锰,问能制得氧气多少克?
(2)若该3.18克固体中有一定量未溶解的氯化钾,求该室温时氯化钾的溶解度和原混合物中氯酸钾的质量分数?
分析 根据氯酸钾在二氧化锰的催化作用下生成氯化钾和氧气,然后结合题中的数据进行解答.
解答 解:(1)3.18克全是MnO2,所以KClO3为12g-3.18g=8.82g,
设生成氧气质量为x
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
8.82g x
$\frac{245}{8.82g}$=$\frac{96}{x}$
x=3.456g
(2)2g水中溶解的氯化钾质量为:3.82g-3.18g=0.64g
设氯化钾的溶解度是y,
$\frac{2g}{0.64g}$=$\frac{100g}{y}$
y=32g
所以14.6g水中溶解的氯化钾质量为z
$\frac{100g}{32g}$=$\frac{14.6g}{z}$
z=4.672g
所以产生的氧气质量为:12g-4.672g-3.82g=3.508g
设参加反应的氯酸钾质量为m
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
245 96
m 3.508g
$\frac{245}{m}$=$\frac{96}{3.508g}$
m=8.953g
所以原混合物中氯酸钾的质量分数为:$\frac{8.593g}{12g}$×100%=74.6%.
故答案为:(1)3.456g;
(2)32g,74.6%.
点评 本题是根据化学方程式的计算题,但此题涉及的方程式较多,步骤有点复杂.一需同学们理清做题思路,二需正确写出所需的化学方程式,三计算一定要准确,有了这三点此题就能完整解出.

练习册系列答案
相关题目
12.下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是( )
| A. | 用生石灰制熟石灰 CaO+2H2O═Ca(OH)2 化合反应 | |
| B. | 用氯酸钾和二氧化锰制取氧气 2KClO3$\frac{\underline{MnO_2}}{△}$2Kl+3O2↑ 分解反应 | |
| C. | 用天然气作燃料 CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O 氧化反应 | |
| D. | 用纯碱制烧碱 2KOH+Na2CO3=K2CO3+2NaOH 复分解反应 |
9.下列反应属于分解反应的是( )
| A. | 硫在氧气中燃烧 | B. | 氯酸钾和二氧化锰混合加热制氧气 | ||
| C. | 铁在氧气中燃烧 | D. | 蜡烛燃烧 |
16.某同学在学习了燃烧与燃料的有关知识后,注意到一张纸容易燃烧,而卷成纸团却不易燃烧,联想到细铁丝受热后,在空气中一般只产生红热现象,而在氧气中能剧烈燃烧,于是引发思考,并进行了实验探究.请你协助回答下面有关问题:
【发现问题】:可燃物燃烧的剧烈程度与哪些因素有关呢?
【提出猜想】:猜想①:燃烧的剧烈程度可能与氧气的浓度有关;猜想②:燃烧的剧烈程度可能与可燃物与氧气的接触面积有关.
【验证猜想】:实验报告如下:
【发现问题】:可燃物燃烧的剧烈程度与哪些因素有关呢?
【提出猜想】:猜想①:燃烧的剧烈程度可能与氧气的浓度有关;猜想②:燃烧的剧烈程度可能与可燃物与氧气的接触面积有关.
【验证猜想】:实验报告如下:
| 验证猜想 | 实验操作 | 实验现象 | 实验结论 |
猜想① | 燃烧更剧烈 | ||
猜想② | 燃烧更剧烈 |
6.已知:饱和溶液,不饱和溶液,稀溶液,浓溶液之间的关系如图列说法不正确的是( )
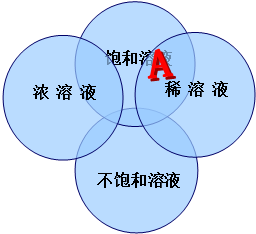

| A. | 图中A处的含义饱和的稀溶液 | |
| B. | 浓溶液一定是饱和溶液,稀溶液一定不饱和 | |
| C. | 在一定的温度下向饱和的硝酸钾溶液中加入少量的硝酸钾晶体,晶体不再溶解 | |
| D. | 同一温度下,同种溶质的饱和溶液一定比它的不饱和溶液浓 |
13.将10g NaOH溶解在100g水中,所得溶液不饱和,该溶液中溶质的质量分数为( )
| A. | 11% | B. | 10% | C. | 9.1% | D. | 1% |
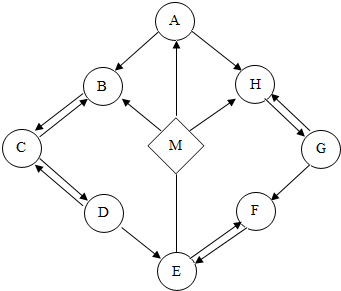
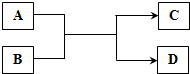 A、B、C、D四种物质在一定条件下有如下转化关系(反应条件已省去).请各写一例符合要求的化学方程式:
A、B、C、D四种物质在一定条件下有如下转化关系(反应条件已省去).请各写一例符合要求的化学方程式: