题目内容
11.(1)实验室用石灰石和稀盐酸反应制取二氧化碳,其发生和收集装置应选用如图中的BC,其中仪器②的名称为长颈漏斗.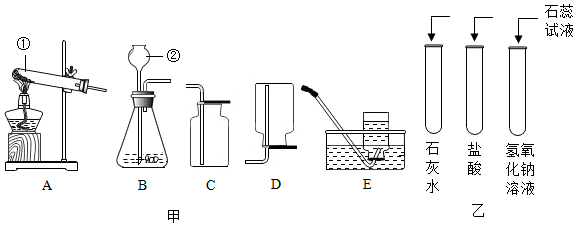
(2)小李同学在做常见酸、碱、与指示剂反应的实验时,所用试剂如图乙所示,实验后他把三支试管中的溶液都倒入干净烧杯中,发现混合液呈红色.则该混合液中含有的溶质有氯化钠、氯化钙、氯化氢.
分析 长颈漏斗方便加液体药品,制取装置包括加热和不需加热两种,实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.如图乙所示,实验后他把三支试管中的溶液都倒入干净烧杯中,发现混合液呈红色,说明盐酸过量,则该混合液中含有的溶质有:氯化钠、氯化钙、氯化氢.
解答 解:(1)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;长颈漏斗方便加液体药品,故答案为:BC;长颈漏斗;
(2)如图乙所示,实验后他把三支试管中的溶液都倒入干净烧杯中,发现混合液呈红色,说明盐酸过量,则该混合液中含有的溶质有:氯化钠、氯化钙、氯化氢;故答案为:氯化钠、氯化钙、氯化氢;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了酸、碱、盐的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
20.下列叙述完全符合质量守恒定律的是( )
| A. | 水结成冰前后,质量保持不变 | |
| B. | 2g氢气在与8g氧气完全反应后可生成10g水 | |
| C. | 1.2g碳与3.2g氧气恰好完全反应可生成4.4g二氧化碳 | |
| D. | 在100g氢氧化钙溶液中,含有1g氢氧化钙和99g水 |





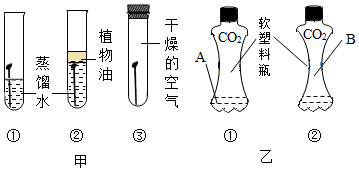 某科学兴趣小组同学在实验时做了如下两实验,现请你回答下列问题
某科学兴趣小组同学在实验时做了如下两实验,现请你回答下列问题