题目内容
16.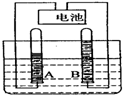 如图是水电解实验的示意图:
如图是水电解实验的示意图:(1)由实验现象确定A端接电池负极
(2)A试管里产生的是氢气;A、B两试管中气体的体积比是2:1;质量比为1:8;B试管里的气体可用带火星的木条来检验.
(3)该反应的化学方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
分析 电解水时通直流电,正极生成的气体是氧气,能使带火星的木条复燃,负极生成氢气,是正极气体体积的2倍,此实验证明是水的元素组成和化学变化的实质.
解答 解:(1)由电解水的装置可知,实验现象是A管产生的气体多,是氢气,可确定A端接电池负极;
(2)由上述分析可知,A试管里产生的是氢气;A、B两试管中气体的体积比是2:1;质量比为1:8;B试管里的气体是氧气,具有助燃性,可用带火星的木条来检验.
(3)电解水生成了氢气和氧气,反应的化学方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
故答为:(1)负;(2)氢,2:1;1:8;B带火星的木条.(3):2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
点评 同学们要熟悉电解水的实验现象和结论,并据此来解决一些常见的问题,此题难度较小.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
4.根据下面四种粒子的结构示意图判断,以下说法正确的是( )
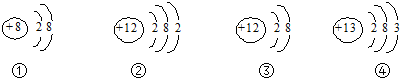
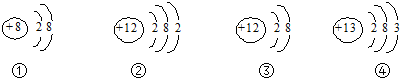
| A. | ①图是一种稀有气体元素的原子结构示意图 | |
| B. | ②图所示的粒子是一种离子 | |
| C. | ②③图所示的粒子化学性质相似 | |
| D. | ③④两图表示的是两种不同元素的微粒 |
11.“春蚕到死丝方尽,蜡炬成灰泪始干”用来比喻老师无私奉献精神,其中也蕴含着很多化学含义.下列说法中不正确的是( )
| A. | 诗句中涉及了化学变化 | |
| B. | 诗句中的“丝”含有的物质是维生素 | |
| C. | 诗句中的“灰”指的是蜡烛燃烧产生的CO2等气体和炭粒 | |
| D. | 诗句中的“泪”指的是液态石蜡 |
5.某化学反应前后的微观示意图如图所示,下列说法正确的是( )

| A. | 该反应是置换反应 | |
| B. | 该反应有2种生成物 | |
| C. | 每个生成物分子由3个原 子构成 | |
| D. | 参加反应的“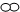 ”和“ ”和“ ”分子的个数比是 3:1 ”分子的个数比是 3:1 |

 某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);
某兴趣小组利用如图所示装置测定石灰石样品中碳酸钙的质量分数,探究过程如下(注:石灰石样品中的杂质不参与反应也不溶解);
