题目内容
某气体样品可能含有NO、N2O5、NO2中的一种或几种,经实验测定该样品中,氮、氧两种元素的质量比为7:16.其样品的组成不可能是( )
| A、NO、NO2和N2O5 |
| B、N2O5和NO |
| C、N2O5和NO2 |
| D、NO2 |
考点:元素质量比的计算
专题:化学式的计算
分析:根据NO中氮元素和氧元素的质量比为14:16=7:8;
N2O5 中氮元素和氧元素的质量比为(14×2):(16×5)=7:20;
NO2 中氮元素和氧元素的质量比为7:16;
混合物中氮元素和氧元素的质量比为7:16,由此可知混合物中NO2的质量可以为任意值.
N2O5 中氮元素和氧元素的质量比为(14×2):(16×5)=7:20;
NO2 中氮元素和氧元素的质量比为7:16;
混合物中氮元素和氧元素的质量比为7:16,由此可知混合物中NO2的质量可以为任意值.
解答:解:A.根据NO、N2O5、NO2中氮元素和氧元素的质量比,NO中氮元素和氧元素的质量比为7:8>7:16;N2O5 中氮元素和氧元素的质量比为7:20<7:16;NO2混合物中氮元素和氧元素的质量比为7:16;故可能;
B.N2O5 中氮元素和氧元素的质量比为7:20;NO中氮元素和氧元素的质量比为7:8;故两者混合可能为7:16;故可能;
C.N2O5 中氮元素和氧元素的质量比为7:20;NO2中氮元素和氧元素的质量比为7:16;故两者混合不可能为7:16;故不可能;
D.NO2 中氮元素和氧元素的质量比为7:16;故可能;
故选C.
B.N2O5 中氮元素和氧元素的质量比为7:20;NO中氮元素和氧元素的质量比为7:8;故两者混合可能为7:16;故可能;
C.N2O5 中氮元素和氧元素的质量比为7:20;NO2中氮元素和氧元素的质量比为7:16;故两者混合不可能为7:16;故不可能;
D.NO2 中氮元素和氧元素的质量比为7:16;故可能;
故选C.
点评:本题考查学生根据化合物中元素的质量比进行分析解题的能力;有两种或者是三种的话一定要一个比这个比例大,一个比这个比例小,混合物才能符合样品比例的条件.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质的用途,主要利用了物质的化学性质的是( )
| A、氧气用于急救病人 |
| B、“干冰”用于人工降雨 |
| C、稀有气体用于电光源 |
| D、铜用于制造导线 |
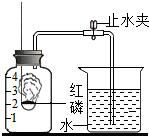 某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下:
某同学设计了测定空气中氧气含量的实验,实验装置如图.该同学的实验步骤如下: