题目内容
13克锌和100克稀硫酸刚好完全反应.求:
(1)生成的氢气质量;
(2)硫酸溶液中溶质的质量分数.
(1)生成的氢气质量;
(2)硫酸溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:(1)根据锌的质量求出反应生成氢气的质量、参加反应的硫酸溶液中溶质的质量以及生成硫酸锌的质量进行解答;
(2)根据溶质质量分数公式求出硫酸溶液中溶质的质量分数即可;
(2)根据溶质质量分数公式求出硫酸溶液中溶质的质量分数即可;
解答:解:(1)设参加反应的H2SO4的质量为x,生成氢气的质量为y
Zn+H2SO4=ZnSO4+H2↑
65 98 2
13g x y
=
=
x=19.6g y=0.4g
(2)这种硫酸溶液中溶质的质量分数=
=19.6%
答:(1)生成的氢气质量是0.4g; (2)硫酸溶液中溶质的质量分数为19.6%;
Zn+H2SO4=ZnSO4+H2↑
65 98 2
13g x y
| 65 |
| 13g |
| 98 |
| x |
| 2 |
| y |
x=19.6g y=0.4g
(2)这种硫酸溶液中溶质的质量分数=
| 16.9g |
| 100g |
答:(1)生成的氢气质量是0.4g; (2)硫酸溶液中溶质的质量分数为19.6%;
点评:本题主要考查学生对物质质量分数和溶质质量分数的计算能力.学生需正确书写出化学方程式,并能正确运用溶质质量分数公式进行计算,才能正确答题.

练习册系列答案
相关题目
以下说法正确的是( )
①CO是一种有毒的气体,它有害无利
②易燃易爆物应露天存放,紧密堆积
③燃烧固体燃料需要架空,目的是增大可燃物与空气的接触面积
④三大化石燃料是指煤、石油、天然气
⑤造成酸雨的主要气体是SO2和CO2.
①CO是一种有毒的气体,它有害无利
②易燃易爆物应露天存放,紧密堆积
③燃烧固体燃料需要架空,目的是增大可燃物与空气的接触面积
④三大化石燃料是指煤、石油、天然气
⑤造成酸雨的主要气体是SO2和CO2.
| A、①②④ | B、①③④ |
| C、③④ | D、③④⑤ |
下列四种图示的方法读量筒内液体的体积数,其中正确的是( )
A、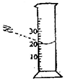 |
B、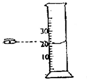 |
C、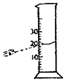 |
D、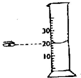 |
下列说法中正确的是( )
| A、氧化物都是化合物 |
| B、氧化物只能由物质跟氧气反应生成 |
| C、凡含有氧元素的化合物都是氧化物 |
| D、氧化物的名称都有氧字,如“二氧化碳”“氧化钙”等 |
人们的日常生活离不开水,水是一种( )
| A、混合物 | B、化合物 |
| C、单质 | D、元素 |
有三瓶无色无味的气体,分别是氧气、空气、氮气,区别它们最简单的方法是( )
| A、测定气体的密度 |
| B、分别倒入澄清石灰水 |
| C、分别伸入燃着的木条 |
| D、闻气体气味 |
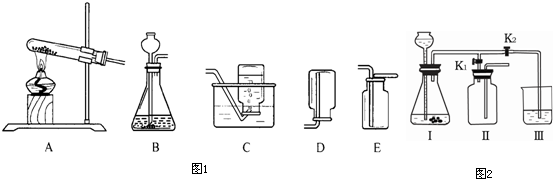
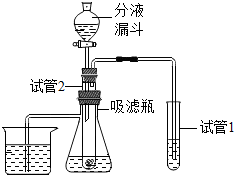 某化研究性学习小组的同学们做了三个趣味实验,装置如图(气密性良好).当开启分液漏斗的旋塞,液体滴入盛有固体的试管2中时,观察不同的现象.
某化研究性学习小组的同学们做了三个趣味实验,装置如图(气密性良好).当开启分液漏斗的旋塞,液体滴入盛有固体的试管2中时,观察不同的现象.