题目内容
12.根据化学性质不同,氧化物主要可分为酸性氧化物、碱性氧化物、两性氧化物和不成盐氧化物.凡能跟碱反应,生成盐和水的氧化物交酸性氧化物;能跟酸反应,生成盐和水的氧化物,叫做碱性氧化物.Al2O3是一种两性氧化物,它有如下化学性质:Al2O3+6HCl═2AlCl3+3H2O;Al2O3+2NaOH═2NaAlO2+H2O 请回答下列问题:
(1)下列氧化物中,属于酸性氧化物的是C.(填字母编号)
A.H2O B.CO C.SO2 D.Fe2O3
(2)NaAlO2的名称是偏铝酸钠,它属于盐(选填“酸”、“碱”、“盐”或“氧化物”).偏铝酸钠电离时产生的阴离子是AlO2-(填离子符号).
分析 (1)根据能跟酸反应,生成盐和水的氧化物,叫做碱性氧化物考虑;
(2)根据偏铝酸钠的构成分析.
解答 解:(1)酸性氧化物是与碱反应生成盐和水的氧化物,水、一氧化碳、氧化铁都不能与碱反应,故选C;
(2)偏铝酸钠由钠离子和偏铝酸根离子构成,所以属于盐,电离时产生的阴离子是AlO2-.
故答案为:(1)C;(2)盐;AlO2-.
点评 解答本题关键是从题干中提取有用信息,并能灵活运用.

练习册系列答案
 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 小学教材完全解读系列答案
小学教材完全解读系列答案
相关题目
4.H2SO4中加入下列哪种物质会发生中和反应并出现白色沉淀( )
| A. | NaOH | B. | BaCl2 | C. | Ba(OH)2 | D. | CuO |
3.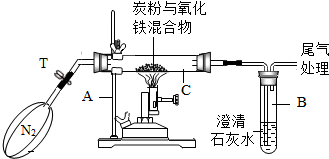 某化学兴趣小组的学生研究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:
某化学兴趣小组的学生研究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:
(1)提出假设:气体产物全部是CO2.
(2)查阅资料:a.氮气不能与炭粉及Fe2O3反应.
b.高温下可以发生下列反应:2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑,C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO
(3)设计方案:将一定量氧化铁在隔绝空气的环境下与过量炭粉充分反应.用实验中实际测得产生气体的质量,与理论计算得到的CO2的质量进行比较.
(4)实验装置:如图所示.
(5)实验操作:
①称量:反应前Fe2O3的质量3.20g;炭粉的质量2.00g;玻璃管C的质量48.48g.反应后玻璃管与残留固体共52.24g.
②加热前先通一段时间氮气,再夹紧弹簧夹T,点燃酒精喷灯加热.
(6)问题分析:①用酒精喷灯而不用酒精灯的目的是获取反应所需的高温条件.
②加热前先通一段时间氮气的目的是清除试管中空气(氧气),防止炭粉与空气中氧气发生反应.
③理论计算:若氧化铁与炭粉反应的气体产物全部是CO2,求3.20g氧化铁完全反应时生成CO2的质量.(写出计算过程)
④根据实验数据计算实验中实际获得气体的质量.(写出计算过程)
(7)结论:原假设不能(能、不能)成立,理由是因为生成的气体质量为1.44g,大于1.32g,故气体产物不完全为CO2,实际是C02和C0的混合物,原假设不能成立.
(8)兴趣小组成员小聪想到家里新换的水龙头.他从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你参与.
【作出猜想】
猜想1:Cr>Fe>Cu;
猜想2:Fe>Cu>Cr;
猜想3:你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
【结论与解释】
①小聪得到的结论是猜想1正确.
②实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出化学方程式Cr+FeSO4=Fe+CrSO4.
 某化学兴趣小组的学生研究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:
某化学兴趣小组的学生研究过量的炭粉与Fe2O3在高温条件下反应的气体产物成分.探究过程如下:(1)提出假设:气体产物全部是CO2.
(2)查阅资料:a.氮气不能与炭粉及Fe2O3反应.
b.高温下可以发生下列反应:2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑,C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO
(3)设计方案:将一定量氧化铁在隔绝空气的环境下与过量炭粉充分反应.用实验中实际测得产生气体的质量,与理论计算得到的CO2的质量进行比较.
(4)实验装置:如图所示.
(5)实验操作:
①称量:反应前Fe2O3的质量3.20g;炭粉的质量2.00g;玻璃管C的质量48.48g.反应后玻璃管与残留固体共52.24g.
②加热前先通一段时间氮气,再夹紧弹簧夹T,点燃酒精喷灯加热.
(6)问题分析:①用酒精喷灯而不用酒精灯的目的是获取反应所需的高温条件.
②加热前先通一段时间氮气的目的是清除试管中空气(氧气),防止炭粉与空气中氧气发生反应.
③理论计算:若氧化铁与炭粉反应的气体产物全部是CO2,求3.20g氧化铁完全反应时生成CO2的质量.(写出计算过程)
④根据实验数据计算实验中实际获得气体的质量.(写出计算过程)
(7)结论:原假设不能(能、不能)成立,理由是因为生成的气体质量为1.44g,大于1.32g,故气体产物不完全为CO2,实际是C02和C0的混合物,原假设不能成立.
(8)兴趣小组成员小聪想到家里新换的水龙头.他从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你参与.
【作出猜想】
猜想1:Cr>Fe>Cu;
猜想2:Fe>Cu>Cr;
猜想3:你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 | 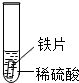 | 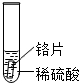 | 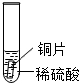 |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 铜表面无气泡 |
①小聪得到的结论是猜想1正确.
②实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出化学方程式Cr+FeSO4=Fe+CrSO4.
20.关于下列四种粒子的说法中,不正确的是( )
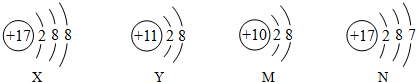
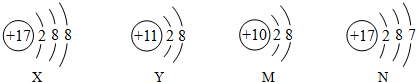
| A. | 以上四种粒子分别属于三种元素 | |
| B. | 粒子Y若得到1个电子就可以变成原子 | |
| C. | 如果X和Y能形成稳定的化合物,则化学式应为XY | |
| D. | 上述粒子中有两个是离子,两个是原子 |
4.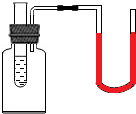 如图所示,集气瓶瓶塞中插有小试管和导管,小试管中盛有少量水,导管连接的U型管两侧内水面持平.向试管中加入下列物质中的一种,U型管两侧水面出现左低右高,则加入的物质为①CaO②NaOH③NaCl④硝酸铵⑤浓H2SO4( )
如图所示,集气瓶瓶塞中插有小试管和导管,小试管中盛有少量水,导管连接的U型管两侧内水面持平.向试管中加入下列物质中的一种,U型管两侧水面出现左低右高,则加入的物质为①CaO②NaOH③NaCl④硝酸铵⑤浓H2SO4( )
 如图所示,集气瓶瓶塞中插有小试管和导管,小试管中盛有少量水,导管连接的U型管两侧内水面持平.向试管中加入下列物质中的一种,U型管两侧水面出现左低右高,则加入的物质为①CaO②NaOH③NaCl④硝酸铵⑤浓H2SO4( )
如图所示,集气瓶瓶塞中插有小试管和导管,小试管中盛有少量水,导管连接的U型管两侧内水面持平.向试管中加入下列物质中的一种,U型管两侧水面出现左低右高,则加入的物质为①CaO②NaOH③NaCl④硝酸铵⑤浓H2SO4( )| A. | ②或③或⑤ | B. | ①或③或⑤ | C. | ①或②或④ | D. | ①或②或⑤ |
2.下列属于置换反应的是( )
| A. | 制漂白粉2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O | |
| B. | 潜艇供氧2Na2O2+2H2O=4NaOH+O2↑ | |
| C. | 高炉炼铁3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 | |
| D. | 焊接铁轨2Al+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+Al203 |
 金属及合金是重要的化工材料.
金属及合金是重要的化工材料.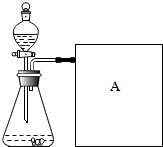 研究性学习小组进行“影响过氧化氢生成O2快慢的有关因素”的课题探究.以下是他们探究的主要过程:
研究性学习小组进行“影响过氧化氢生成O2快慢的有关因素”的课题探究.以下是他们探究的主要过程: