题目内容
19. 某校化学兴趣小组就空气中氧气的含量进行实验探究:
某校化学兴趣小组就空气中氧气的含量进行实验探究:【收集资料】硫是一种淡黄色固体,在空气中点燃时能与氧气发生反应生成二氧化硫(表达式:S+O2→SO2).SO2是一种有刺激性气味的气体,易溶于水.
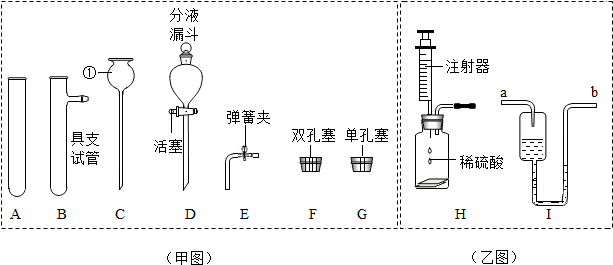
【设计实验】第一小组同学选择的药品是足量的红磷,设计了如图1装置.
(1)红磷在燃烧时的主要现象是发黄光、放出热量、冒出大量的白烟.
(2)燃烧完毕,冷却至室温后打开止水夹,看到的现象是水进入集气瓶约占瓶内空气体积的五分之一.
(3)一般不用木炭的原因是木炭燃烧生成二氧化碳,内外压强变化不大.
(4)集气瓶中红磷燃烧的表达式是磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
| 步骤 | 现象 |
| ①用燃烧匙将硫点燃后伸入到大试管中,立即密封. | 硫燃烧 |
| ②待硫熄灭后,将试管倒立于 盛有冷水的水槽中,并在水中将橡皮塞取下.如图2 | 一段时间后,试管中上升了一段稳定的水柱,水约占试管容积的$\frac{1}{5}$ |
(6)最终水约占试管容积的$\frac{1}{5}$,该实验的结论是氧气约占空气体积的五分之一.
(7)如果不足$\frac{1}{5}$,可能是下列原因中的ABC(填字母).
A.硫用量不足B.未冷却至室温C.气密性不好
(8)取试管中液体放入另一支试管中,在空气中放置一段时间,然后加入紫色石蕊试液,紫色石蕊试液变为红色,说明其中生成了酸性物质--硫酸.请写出硫酸的化学式H2SO4.给它加热,发现它不变为紫色,请你推测硫酸的一个化学性质硫酸受热不易分解.
分析 本题是测定氧气在空气中的体积分数的实验探究,要把空气中的氧气消耗掉,在本实验中用的是红磷;红磷在空气中燃烧的现象:发黄光、放出热量、冒出大量的白烟.燃烧完毕,冷却至室温后打开止水夹,看到的现象是:水进入集气瓶约占瓶内空气体积的五分之一;一般不用木炭的原因是:木炭燃烧生成二氧化碳,内外压强变化不大;由表格信息可知,水上升的原因是:二氧化硫溶于水,使内外形成压强差;因为一段时间后,试管中上升了一段稳定的水柱,水约占试管容积的$\frac{1}{5}$,所以氧气约占空气体积的五分之一;保证本实验成功的关键是:①装置的气密性好;②硫粉足量;③必须冷却到室温再读数;否则结果偏小.一个硫酸分子是由两个氢原子、一个硫原子和四个氧原子构成的,给它加热,发现它不变为紫色,推测硫酸的一个化学性质是:硫酸受热不易分解.
解答 解:(1)红磷在空气中燃烧的现象:发黄光、放出热量、冒出大量的白烟;故答案为:发黄光、放出热量、冒出大量的白烟;
(2)燃烧完毕,冷却至室温后打开止水夹,看到的现象是:水进入集气瓶约占瓶内空气体积的五分之一;故答案为:水进入集气瓶约占瓶内空气体积的五分之一;
(3)一般不用木炭的原因是:木炭燃烧生成二氧化碳,内外压强变化不大,故答案为:木炭燃烧生成二氧化碳,内外压强变化不大;
(4)红磷和氧气在点燃的条件下生成五氧化二磷,故答案为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(5)由表格信息可知,水上升的原因是:二氧化硫溶于水,使内外形成压强差;故答案为:二氧化硫溶于水,使内外形成压强差;
(6)因为一段时间后,试管中上升了一段稳定的水柱,水约占试管容积的$\frac{1}{5}$,所以氧气约占空气体积的五分之一;故答案为:氧气约占空气体积的五分之一;
(7)保证本实验成功的关键是:①装置的气密性好;②硫粉足量;③必须冷却到室温再读数;否则结果偏小,故答案为:ABC
(8)一个硫酸分子是由两个氢原子、一个硫原子和四个氧原子构成的,给它加热,发现它不变为紫色,推测硫酸的一个化学性质是:硫酸受热不易分解;故答案为:H2SO4;硫酸受热不易分解;
答案:
(1)发黄光、放出热量、冒出大量的白烟;
(2)水进入集气瓶约占瓶内空气体积的五分之一;
(3)木炭燃烧生成二氧化碳,内外压强变化不大;
(4)磷+氧气$\stackrel{点燃}{→}$五氧化二磷;
(5)二氧化硫溶于水,使内外形成压强差;
(6)氧气约占空气体积的五分之一;
(7)ABC;
(8)H2SO4;硫酸受热不易分解;
点评 本考点是用白磷测定氧气在空气中的体积分数,属于实验方法和过程的探究.要使本实验成功,必须注意以下几点:①装置的气密性好;②红磷足量;③必须冷却到室温再读数.本考点主要出现在填空题和实验题中.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 石灰水 | B. | 黄铜 | C. | 铁锈 | D. | 高锰酸钾 |
| 实验次数 | O2的质量 | 生成CO2质量 |
| 第一次 | 24g | 33g |
| 第二次 | 32g | 44g |
| 第三次 | 36g | 44g |
(2)第一次实验木炭有剩余,剩余3g.
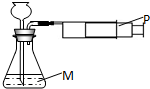
| A. | 向外缓缓拉时可见漏斗下端有气泡 | |
| B. | 向内缓缓推时可见漏斗下端有气泡 | |
| C. | M是澄清石灰水,注射器中充满CO2,观察到P右移 | |
| D. | M是无色酚酞试液,注射器中充满氨气,观察到锥形瓶液体变红 |
| A. | CO和CO2 | B. | CO和H2 | C. | 面粉和空气 | D. | CO2和O2 |
| A. | 冰水混合物 | B. | 天然气 | C. | 清澈的泉水 | D. | 不锈钢 |