题目内容
3.下列说法正确的是( )| A. | 配置溶液时,只能用水做溶剂 | |
| B. | 氯化钠溶于水时,溶液温度升高 | |
| C. | 酒精跟水以任意比互相溶解时,酒精做溶质,水做溶剂 | |
| D. | 乳化就是溶解 |
分析 A、根据汽油、酒精都可以做溶剂解答;
B、根据物质溶解时伴随着放热、吸热现象进行分析解答;
C、根据有水时,不管量多量少,一般把水看作溶剂解答;
D、根据乳化作用以及溶解的概念进行分析.
解答 解:A、碘酒中溶质是碘,溶剂是酒精,所以溶液中的溶剂不一定是水,故错误;
B、物质溶解时伴随着放热、吸热现象,溶质在溶解过程中,有的放出热量(如NaOH、浓H2SO4),有的吸收热量(如NH4NO3),氯化钠溶于水时,溶液温度基本不变,故错误;
C、有水时,不管量多量少,一般把水看作溶剂,酒精跟水相互溶解时,酒精作为溶质,水作为溶剂,故选项说法正确;
D、乳化作用与溶解最大的不同是混合物中分散的物质形式不同,前者以小液滴形式分散,后者以分子或离子形式分散,故错误.
故选C.
点评 本题难度不大,掌握溶液的组成、物质溶解时放热与吸热现象以及乳化作用的概念等是正确解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
14.某化学兴趣活动小组的同学作了以下两个探究实验:
(1)探究影响化学反应速率的因素:在实验室制取二氧化碳的研究中,进行了如下实验:
①实验室制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应速率的影响,可选择实验甲与实验乙(选填实验编号)进行对照实验.
③若要研究反应物的接触面积对反应速率的影响,可选择实验甲与实验丙(选填实验编号)进行对照实验.
④化学反应的实质是微观粒子相互接触、碰撞的结果,试从微观角度解释“反应物的接触面积越大,化学反应速率越快”的原因是:反应物浓度越大,单位体积的反应物中含有的粒子数越多,粒子间碰撞的概率越大,化学反应速率越快.
⑤乙和丁相比较,产生气体的速率较快的是丁,完全反应后,产生二氧化碳的质量相等(填“相等”或“不等”).
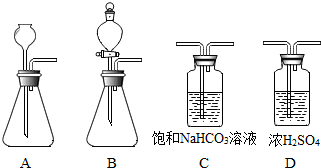
⑥若要选择了这组药品制取二氧化碳,为了能得到较平稳的气流,应选择如图装置中的B(填“A”或“B”),理由是分液漏斗可以控制盐酸加入的速率,从而控制反应的速率.由于浓盐酸具有强烈的挥发性,会导致收集到的二氧化碳中含有氯化氢气体,为了得到干燥、纯净的二氧化碳,可将产生的二氧化碳依次通过下列装置C、D.(温馨提示:①浓硫酸具有吸水性,可作干燥剂;②二氧化碳不与饱和NaHCO3溶液反应,氯化氢可与之反应,相应的化学方程式:NaHCO3+HCl═NaCl+H2O+CO2↑)
(2)探究二氧化碳与氢氧化钠的反应.
通过查阅资料可知:①氢氧化钠与氢氧化钙的化学性质相似,其水溶液也能与二氧化碳反应.②通常情况下,1体积水能溶解1体积二氧化碳.
二氧化碳通入澄清石灰水,石灰水变浑浊,相应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O,某同学将二氧化碳通入氢氧化钠溶液,无明显现象,模仿二氧化碳与氢氧化钙反应的化学方程式,写出二氧化碳与氢氧化钠反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
对于无明显现象的化学反应,可通过验证反应物的减少或生成物的存在来证明发生了化学反应,某同学根据这个原则设计了三个实验方案验证二氧化碳确与氢氧化钠溶液发生了化学反应.
其中方案二(写出方案编号)不能证明二氧化碳确与氢氧化钠反应了,理由是二氧化碳能够溶于水,导致塑料瓶中压强减小,从而导致塑料瓶变瘪.
| 试液编号药品 | 甲 | 乙 | 丙 | 丁 |
| 大理石 | mg,块状 | mg,块状 | mg,粉末状 | mg,粉末状 |
| 盐酸(过量) | wg,稀盐酸 | wg,浓盐酸 | wg,稀盐酸 | wg,浓盐酸 |
①实验室制取二氧化碳的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
②若要研究盐酸浓度大小对反应速率的影响,可选择实验甲与实验乙(选填实验编号)进行对照实验.
③若要研究反应物的接触面积对反应速率的影响,可选择实验甲与实验丙(选填实验编号)进行对照实验.
④化学反应的实质是微观粒子相互接触、碰撞的结果,试从微观角度解释“反应物的接触面积越大,化学反应速率越快”的原因是:反应物浓度越大,单位体积的反应物中含有的粒子数越多,粒子间碰撞的概率越大,化学反应速率越快.
⑤乙和丁相比较,产生气体的速率较快的是丁,完全反应后,产生二氧化碳的质量相等(填“相等”或“不等”).
⑥若要选择了这组药品制取二氧化碳,为了能得到较平稳的气流,应选择如图装置中的B(填“A”或“B”),理由是分液漏斗可以控制盐酸加入的速率,从而控制反应的速率.由于浓盐酸具有强烈的挥发性,会导致收集到的二氧化碳中含有氯化氢气体,为了得到干燥、纯净的二氧化碳,可将产生的二氧化碳依次通过下列装置C、D.(温馨提示:①浓硫酸具有吸水性,可作干燥剂;②二氧化碳不与饱和NaHCO3溶液反应,氯化氢可与之反应,相应的化学方程式:NaHCO3+HCl═NaCl+H2O+CO2↑)

(2)探究二氧化碳与氢氧化钠的反应.
通过查阅资料可知:①氢氧化钠与氢氧化钙的化学性质相似,其水溶液也能与二氧化碳反应.②通常情况下,1体积水能溶解1体积二氧化碳.
二氧化碳通入澄清石灰水,石灰水变浑浊,相应的化学方程式为CO2+Ca(OH)2=CaCO3↓+H2O,某同学将二氧化碳通入氢氧化钠溶液,无明显现象,模仿二氧化碳与氢氧化钙反应的化学方程式,写出二氧化碳与氢氧化钠反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
对于无明显现象的化学反应,可通过验证反应物的减少或生成物的存在来证明发生了化学反应,某同学根据这个原则设计了三个实验方案验证二氧化碳确与氢氧化钠溶液发生了化学反应.
| 方案编号 | 方案 | 实验现象 | 结论 |
| 一 | 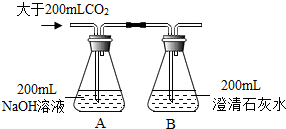 | A、B瓶均无明显现象 | 二氧化碳确与氢氧化钠反应了 |
| 二 | 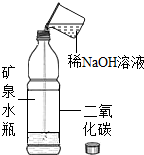 加入NaOH溶液后,盖好瓶盖,振荡 | 塑料瓶变瘪 | 二氧化碳确与氢氧化钠反应了 |
| 三 | 往二氧化碳和氢氧化钠溶液作用后的液体中加入稀盐酸 | 有气泡产生 | 二氧化碳确与氢氧化钠反应了 |
8.下列各组物质里,前者是后者的溶质的是( )
| A. | 生石灰、石灰水 | B. | 酒精、碘酒 | ||
| C. | 氯化氢、盐酸 | D. | 二氧化碳、碳酸溶液 |
15.蜡烛燃烧时,我们会看到许多现象,一下不是蜡烛燃烧现象的是( )
| A. | 蜡烛流泪 | B. | 火焰分三层 | ||
| C. | 生成二氧化碳和水 | D. | 生成黑烟 |
12.振荡试管的正确操作是( )
| A. | 用手紧握试管上下晃动 | B. | 用手指拿住试管用腕摆动 | ||
| C. | 用拇指堵住试管口上下晃动 | D. | 用手紧握试管用臂摆动 |
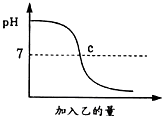 酸与碱作用生成盐和水的反应叫做中和反应.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向甲中加入乙时溶液pH的变化曲线.请写出你从曲线图中所获取的信息:
酸与碱作用生成盐和水的反应叫做中和反应.已知甲、乙分别是盐酸溶液和氢氧化钠溶液中的一种,如图表示向甲中加入乙时溶液pH的变化曲线.请写出你从曲线图中所获取的信息: