题目内容
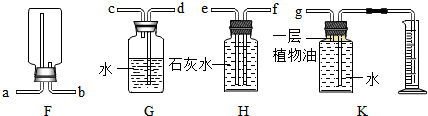
7.某化学兴趣小组利用所学化学知识进行如下实验(夹持仪器已省略,假设气体均吸收完全).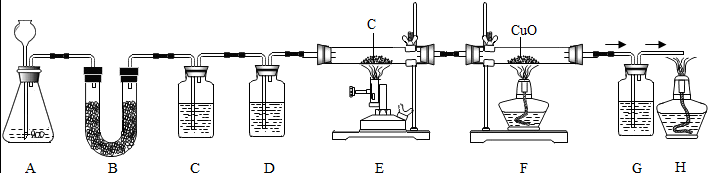
以上装置的目的是制取CO,并探究CO的相关性质,请完成下列问题:
①写出大理石与稀盐酸在A中发生反应的化学方程式:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②从A中出来的气体CO2中含有两种杂质,B装置能检验其中一种杂质,请说明杂质气体通过B装置时,所用试剂的化学式CuSO4;装置D中的试剂为浓硫酸,请问浓硫酸在此处的作用是:除去混合气体中的水蒸气;
③在E、F处加热之前,需通入一段时间CO2的目的是排净装置内的空气;
④尾部H处放置一点燃的酒精灯的目的是点燃尾气中的一氧化碳,以免造成空气的污染.
分析 ①首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可;
②从A中出来的气体CO2中含有氯化氢气体和水蒸气;
③装置内充满了空气,以免生成的一氧化碳与之混合加热发生爆炸;
④根据尾气中含有一氧化碳来分析.
解答 解:①大理石与稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
②无水硫酸铜遇水变蓝色,所以可用无水硫酸铜来检验水蒸气的存在,浓硫酸具有吸水性,可以除去混合气体中的水蒸气;故填:CuSO4;除去混合气体中的水蒸气;③装置内充满了空气,若E生成的一氧化碳与之混合,加热有发生爆炸的危险;故填:排净装置内的空气;
④尾气中含有有毒的一氧化碳气体,直接排放到空气中会造成污染,故填:点燃尾气中的一氧化碳,以免造成空气的污染.
点评 解答本题的关键是要充分理解实验装置的特点和各种物质的性质,只有这样才能对问题做出正确的判断.

练习册系列答案
相关题目
17.下列离子能在pH=12的溶液中大量共存的一组是( )
| A. | Na+、SO4+、OH-、Ba2+ | B. | K+、NH4+、CO32-、Cl- | ||
| C. | Na+、Cu2+、Cl- SO42- | D. | Na+、Ca2+、Cl-、NO3- |
15.下列有关物质性质叙述正确的是( )
| A. | CO2、CO组成相同,故密度相同 | |
| B. | H2SO4溶液能使紫色石蕊试液变红 | |
| C. | 已知NaHSO4溶液呈酸性,故该物质属于酸 | |
| D. | 向稀硫酸中加入少量Ag粉,会有气泡生成 |
2.写出下列符号中“2”所表示的含义
Mg2+一个镁离子带有两个单位的正电荷;$\stackrel{+2}{Cu}$铜元素的化合价为+2价;
2S硫原子的个数为2;SO21个二氧化硫分子中含有2个氧原子.
Mg2+一个镁离子带有两个单位的正电荷;$\stackrel{+2}{Cu}$铜元素的化合价为+2价;
2S硫原子的个数为2;SO21个二氧化硫分子中含有2个氧原子.
19.下列食品的处理方法不符合《食品添加剂使用卫生标准》的是( )
| A. | 做菜时用铁强化酱油调味 | |
| B. | 在煲好的骨头汤中放入适量加碘食盐 | |
| C. | 凉拌黄瓜时滴入少许麻油 | |
| D. | 为保持肉制品鲜美加入过量的亚硝酸钠 |
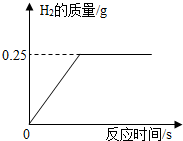 硅钢合金是变压器、充电器中的核心材料,其主要成份是铁和硅.向8.4g硅钢中加入100g稀硫酸,恰好完全反应(硅及其杂质不溶于水,且都不与稀硫酸反应),放出气体的质量与反应时的关系如图所示.
硅钢合金是变压器、充电器中的核心材料,其主要成份是铁和硅.向8.4g硅钢中加入100g稀硫酸,恰好完全反应(硅及其杂质不溶于水,且都不与稀硫酸反应),放出气体的质量与反应时的关系如图所示.