题目内容
8.水中氢、氧两种元素的质量比是1:8.分析 根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,进行解答.
解答 解:根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,可得水中氢元素与氧元素的质量比为:(1×2):16=1:8;
故填:1:8.
点评 本题主要考查学生运用化学式和元素的相对原子质量进行计算的能力,主要是利用了:化合物中各元素质量比=各元素的相对原子质量×原子个数之比的计算公式.

练习册系列答案
相关题目
18.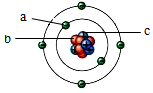 图为某原子结构模型的示意图,其中 a、b、c 是构成该原子的三种不同粒子,下列说法正确的是( )
图为某原子结构模型的示意图,其中 a、b、c 是构成该原子的三种不同粒子,下列说法正确的是( )
 图为某原子结构模型的示意图,其中 a、b、c 是构成该原子的三种不同粒子,下列说法正确的是( )
图为某原子结构模型的示意图,其中 a、b、c 是构成该原子的三种不同粒子,下列说法正确的是( )| A. | 决定该原子种类的粒子是 b | B. | 原子中 b 与 c 的数目一定相同 | ||
| C. | 原子中 a 与 c 的数目一定相同 | D. | 原子的质量集中在 a 和 c 上 |
19.下列化学反应既不是化合反应也不是分解反应的是( )
| A. | 酒精+氧气$\stackrel{点燃}{→}$二氧化碳+水 | B. | 氧化钙+水--氢氧化钙 | ||
| C. | 氢气+氧气$\stackrel{点燃}{→}$水 | D. | 碳酸--水+二氧化碳 |
16.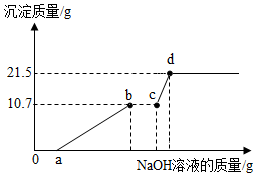 向100g由FeCl3、CuCl2和HCl组成的混合溶液中,慢慢滴加NaOH溶液,边滴边振荡,其反应过程如图所示.已知Fe3+和Cu2+分别开始沉底和完全沉淀时溶液的pH如表
向100g由FeCl3、CuCl2和HCl组成的混合溶液中,慢慢滴加NaOH溶液,边滴边振荡,其反应过程如图所示.已知Fe3+和Cu2+分别开始沉底和完全沉淀时溶液的pH如表
下列判断中正确的是( )
 向100g由FeCl3、CuCl2和HCl组成的混合溶液中,慢慢滴加NaOH溶液,边滴边振荡,其反应过程如图所示.已知Fe3+和Cu2+分别开始沉底和完全沉淀时溶液的pH如表
向100g由FeCl3、CuCl2和HCl组成的混合溶液中,慢慢滴加NaOH溶液,边滴边振荡,其反应过程如图所示.已知Fe3+和Cu2+分别开始沉底和完全沉淀时溶液的pH如表| 离子符号 | 开始沉淀时溶液的pH | 完全沉淀时溶液的pH |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| A. | o~a段、b~c段发生反应的实质都是H++OH-═H2O | |
| B. | a~b段表示Cu2+和OH-反应生成Cu(OH)2沉淀 | |
| C. | c点时溶液中的溶质是CuCl2和NaCl,pH=7 | |
| D. | 原溶液中Fe3+与Cu2+的质量之比为10.7:10.8 |
5.若3.2g某物质在空气中完全燃烧生成4.4g二氧化碳和3.6g水,则下列描述不正确的是( )
| A. | 该物质只含有碳元素和氢元素 | |
| B. | 该物质中碳元素与氢元素的质量比为3:1 | |
| C. | 该物质中碳原子与氢原子的个数比为1:4 | |
| D. | 该物质燃烧消耗氧气的质量为4.8g |
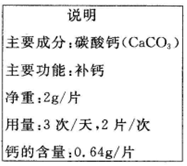 钙片是一种混合物,根据如图某品牌说明书计算:
钙片是一种混合物,根据如图某品牌说明书计算: