题目内容
甲、乙两固体物质的溶解度曲线如图所示,下列说法正确的是( )
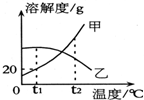

| A、甲物质的溶解度为20g |
| B、t1℃时,30g甲加入到50g水中最多可得70g溶液 |
| C、将t1℃时乙物质的饱和溶液升温t2℃,变成不饱和溶液 |
| D、t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲<乙 |
考点:固体溶解度曲线及其作用,饱和溶液和不饱和溶液相互转变的方法,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、从物质的溶解度与温度有关,题目中没有指明温度去分析解答;
B、从在t1℃时,甲的溶解度为20g,甲在50g水中最多可溶解10g去分析解答;
C、从乙物质的溶解度随温度的升高而降低去分析解答;
D、根据一定温度下,饱和溶液中溶质的质量分数与溶解度的关系去分析解答.
B、从在t1℃时,甲的溶解度为20g,甲在50g水中最多可溶解10g去分析解答;
C、从乙物质的溶解度随温度的升高而降低去分析解答;
D、根据一定温度下,饱和溶液中溶质的质量分数与溶解度的关系去分析解答.
解答:解:A、在t1℃,甲物质的溶解度为20g,题目中没有指明温度;故A错误;
B、由图可知:在t1℃时,甲的溶解度为20g,其意义是在t1℃时,100g水中最多可溶解20g甲物质;那么甲在50g水中最多可溶解10g故可得溶液的质量为50g+10g=60g;故B错误;
C、由于乙物质的溶解度随温度的升高而降低,当将t1℃时乙物质的饱和溶液升温t2℃,乙的溶解度变小,会有晶体析出,溶液仍为饱和溶液;故C错误;
D、根据一定温度下,饱和溶液中溶质的质量分数=
×100%=
×100%,即溶解度越大质量分数也就越大,由上图可知:甲乙两种物质的饱和溶液从t2℃降温至t1℃时,甲有溶质析出,此时甲物质的溶解度为20g;而将降低到t1℃时由于乙溶解度增大而无晶体析出,此时虽然C的溶解度大,但由于不是饱和溶液,所以其溶解的物质还是和先前的t2℃相同,也就是此时计算还是要考虑该t2℃乙物质的溶解度,由上图比较可知在所以在t2℃的溶解度乙物质的溶解度大于20g,故t2℃,甲、乙两物质的饱和溶液分别降温到t1℃时,所得溶液中溶质质量分数的大小关系是:甲<乙;故D正确.
故答案为:D.
B、由图可知:在t1℃时,甲的溶解度为20g,其意义是在t1℃时,100g水中最多可溶解20g甲物质;那么甲在50g水中最多可溶解10g故可得溶液的质量为50g+10g=60g;故B错误;
C、由于乙物质的溶解度随温度的升高而降低,当将t1℃时乙物质的饱和溶液升温t2℃,乙的溶解度变小,会有晶体析出,溶液仍为饱和溶液;故C错误;
D、根据一定温度下,饱和溶液中溶质的质量分数=
| 溶解度 |
| 溶解度+100g |
| 1 | ||
1+
|
故答案为:D.
点评:物质的溶解度与温度有关,没有指明温度无法确定物质的溶解度.

练习册系列答案
相关题目
下列说法正确的是( )
| A、铁元素摄入量不足,会引起坏血病 |
| B、人体缺少微量元素会得病,因此要尽可能多吃含有这些元素的营养补剂 |
| C、碘、钠、氟、锌是人体所需的微量元素 |
| D、幼儿及青少年缺钙会患佝偻病和发育不良 |
下列符号表示两个分子的是( )
| A、2H2 |
| B、H2O |
| C、2H |
| D、Cu+2 |
下列有关氧气的化学性质实验现象的描述,不正确的是( )
| A、磷在氧气中燃烧产生大量的白雾 |
| B、木炭在氧气中燃烧发出白光,放出热量 |
| C、硫在空气中燃烧发出微弱淡蓝色火焰,在氧气中燃烧发出明亮蓝紫色火焰 |
| D、铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 |
在温度超过374℃时,压强超过22.1MPa下的水俗称超临界水(H2O).用超临界水、氧气与聚氯乙烯[(C2H3Cl)n]反应生成无污染的氧化物和一种酸.下列说法正确的是( )
| A、超临界水是一种混合物 |
| B、生成的氧化物中有一氧化碳 |
| C、生成物中的酸是硫酸 |
| D、该反应为解决“白色染污”提供了一种新思路 |
打火机中的液体燃料气化,该变化过程用微粒的观点解释正确的是( )
| A、分子体积变大 |
| B、分子数目增多 |
| C、分子间的间隔变大 |
| D、分子从静止状态变为运动状态 |
下列实验方案或措施中,不合理的是( )
| A、用适量稀盐酸清除铁制品表面的铁锈 |
| B、通过加水过滤除去CaO中混有的CaCO3 |
| C、用CO2鉴别NaOH溶液和Ca(OH)2溶液 |
| D、用水区分氢氧化钠固体和硝酸铵固体 |
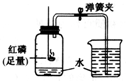 如图所示,用它来测定空气中氧气含量.点燃红磷观察到的现象是
如图所示,用它来测定空气中氧气含量.点燃红磷观察到的现象是