题目内容
16.小明、小强家里蒸馒头用的纯碱中含有少量的氯化钠,聪明好学的他俩决定一起测定该纯碱中碳酸钠的含量.他俩取该纯碱样品16g,加入到273.4g某盐酸溶液中恰好完全反应,同时产生了4.4g气体.试计算:(Na2CO3+2HCl=2NaCl+CO2+H2O)(1)纯碱样品中碳酸钠的质量.
(2)纯碱样品中碳酸钠的质量分数.
分析 碳酸钠和稀盐酸反应生成氯化钠、水和二氧化碳,根据二氧化碳的质量可以计算碳酸钠的质量,进一步可以计算纯碱样品中碳酸钠的质量分数.
解答 解:设碳酸钠的质量为x,
Na2CO3+2HCl═2NaCl+H2O+CO2↑,
106 44
x 4.4g
$\frac{106}{x}$=$\frac{44}{4.4g}$,
x=10.6g,
答:纯碱样品中碳酸钠的质量是10.6g.
(2)纯碱样品中碳酸钠的质量分数为:$\frac{10.6g}{16g}$×100%=66.25%,
答:纯碱样品中碳酸钠的质量分数为66.25%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 百年学典课时学练测系列答案
百年学典课时学练测系列答案 仁爱英语同步练习册系列答案
仁爱英语同步练习册系列答案
相关题目
6.A同学学习化学后知道,镁在氧气中燃烧会生成白色的氧化镁固体.但她在空气中点燃镁条时,却发现在生成的白色固体中还夹杂着少量的淡黄色固体.
[提出问题]为什么会生成淡黄色固体?
[查阅资料]A同学查阅资料,记录了下列几种物质的颜色:
其他同学认为不必查阅氯化镁的颜色,理由是空气中没有含氯元素的物质,不会生成MgCl2;
[提出猜想]分析资料,A认为淡黄色固体可能是由镁与空气中的N2反应生成的;
[实验探究]A设计实验证实了自己的猜想,其方案可能是将镁条放在纯氮气中燃烧.
[实验结论]根据A的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式:
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO、3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
[提出问题]为什么会生成淡黄色固体?
[查阅资料]A同学查阅资料,记录了下列几种物质的颜色:
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 |
| 颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 |
[提出猜想]分析资料,A认为淡黄色固体可能是由镁与空气中的N2反应生成的;
[实验探究]A设计实验证实了自己的猜想,其方案可能是将镁条放在纯氮气中燃烧.
[实验结论]根据A的实验结果,写出镁条在空气中燃烧时两个反应的化学方程式:
2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO、3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2.
7.下列反应属于中和反应的是( )
| A. | CaO+H2O═Ca(OH)2 | B. | Ca(OH)2+H2SO4═CaSO4+2H2O | ||
| C. | 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2 | D. | 2HCl+CuO═CuCl2+H2O |
4.第16界世界气候大会于2011年12月在南非德班召开,会议的主题是“促进低碳经济,减少二氧化碳的排放”.下列做法不符合这一主题的是( )
| A. | 开发新能源(太阳能、潮汐能、风能等),减少化石燃料的使用 | |
| B. | 限制化工发展,关停化工企业,消除污染源头 | |
| C. | 用第四代LED绿色光源代替白炽灯 | |
| D. | 提倡乘坐公共交通工具,骑自行车或步行等出行方式 |
11.下列有关酸的性质说法正确的是( )
| A. | 浓硫酸与浓盐酸都具有吸水性 | |
| B. | 稀硫酸与稀盐酸都可以除铁锈 | |
| C. | 打开盛有浓硫酸与浓盐酸的试剂瓶瓶塞瓶口都有白雾 | |
| D. | 浓硫酸与浓硝酸长期放置液体的质量都会减少 |
1.下列现象是化学变化的是( )
| A. | 铁丝生锈 | B. | 碘的升华 | C. | 石蜡熔化 | D. | 纸张撕裂 |
5.在学习过程中,可以判断反应发生的方法有多种.
(1)向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
当加入氢氧化钠溶液的体积为10mL时,稀盐酸和氢氧化钠溶液恰好完全反应.
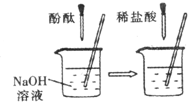
(2)在如图的实验中,当观察到的现象是溶液由红色变为无色 就可证明NaOH与HCl发生了反应.
(3)不使用指示剂或pH试纸等方法,也可证明反应发生.向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是CaCO3.
(1)向盛有10mL稀盐酸的烧杯中加入氢氧化钠溶液,用pH计(测pH的仪器)测定溶液的pH,所得数据如下:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.0 | 7.0 | 11.0 | 12.2 |
(2)在如图的实验中,当观察到的现象是溶液由红色变为无色 就可证明NaOH与HCl发生了反应.

(3)不使用指示剂或pH试纸等方法,也可证明反应发生.向稀盐酸和氢氧化钠混合后的溶液中加入一种物质,若没有明显现象出现,说明溶液失去了酸性,从而证明稀盐酸和氢氧化钠已经发生了反应,则该物质是CaCO3.

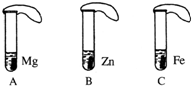 一般情况下,金属越活泼,与酸反应速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图).
一般情况下,金属越活泼,与酸反应速度越快.为了探究金属Mg、Zn、Fe与酸反应的快慢,某研究性学习小组设计了如下实验(如图).