题目内容
20.某环保部门取下降的雨水测定(正常雨水的pH约为5.6,酸雨的pH则不于5.6),其中含有亚硫酸(H2SO3),该酸不稳定,易发生如下反应:2H2SO3+O2═2H2SO4(已知同等条件下亚硫酸比硫酸酸性弱).每隔一段时间测定收集的雨水的pH如下:| 测定时间/分钟 | 0 | 1 | 2 | 4 | 5 |
| pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
| A. | 主要是因为雨水中的成份发生变化,溶液pH发生变化 | |
| B. | 雨水酸性逐渐减弱 | |
| C. | 酸雨可腐蚀某些金属制品 | |
| D. | 酸雨是空气受污染造成的 |
分析 A.根据题意,表格信息进行分析判断.
B.当溶液的pH小于7时,呈酸性,且pH越小,酸性越强.
C.由题意,酸雨中含有酸,根据酸的化学性质进行分析判断.
D.根据酸雨的形成的原因进行分析判断.
解答 解:A.根据题意,雨水中含有亚硫酸(H2SO3),该酸不稳定,在空气中易发生:2H2SO3+O2=2H2SO4(已知同等条件下亚硫酸比硫酸酸性弱),雨水中的成份发生变化,溶液pH发生变化,故选项说法正确.
B.当溶液的pH小于7时,呈酸性,且pH越小,酸性越强,根据题意,雨水的pH逐渐减小,酸性逐渐增强,故选项说法错误.
C.酸雨中含有酸,显酸性,能与金属发生化学反应,可腐蚀某些金属制品,故选项说法正确.
D.二氧化硫、二氧化氮等空气污染物在空气中反应后的生成物溶于雨水形成酸雨,故选项说法正确.
故选B.
点评 本题主要考查了酸雨的产生和危害,掌握溶液的酸碱性和溶液pH大小之间的关系是顺利解题的关键.

练习册系列答案
相关题目
10.下列各图中能说明分子间的间隔变小的是( )
| A. |  炒菜闻到香味 | B. |  湿衣服晾干 | ||
| C. |  酚酞遇氨水变红 | D. |  压缩空气 |
11.有的能源可直接从自然界获取,该类能源叫一次能源;有的不能直接从自然界获取,此类能源叫二次能源.下列属于二次能源的是( )
| A. | 煤 | B. | 石油 | C. | 天然气 | D. | 电能 |
15.将等质量的铁分别跟足量的稀硫酸以及稀盐酸反应,在标准状况下产生氢气的体积( )
| A. | 跟稀硫酸反应产生的氢气多 | B. | 跟盐酸反应产生的氢气多 | ||
| C. | 两者相等 | D. | 无法判断 |
5.小玲同学对所学部分化学知识归纳如下,其中有错误的一组是( )
| A生活中的物质 | B安全常识 | C元素与人体健康 | D日常生活经验 |
| 铅笔芯主要成分石墨 饮水机滤芯的吸附剂主要成分活性炭 | 进入陌生溶洞前先做灯火实验 稀释浓硫酸水倒入浓硫酸中 | 缺铁易引起贫血 缺碘易患甲状腺肿大 | 区别老陈醋与酱油闻气味 区分羊毛纤维与合成纤维灼烧后闻气味 |
| A. | A | B. | B | C. | C | D. | D |
12. 小柯探究pH对唾液淀粉酶活性的影响,其实验过程及结果如下:
小柯探究pH对唾液淀粉酶活性的影响,其实验过程及结果如下:
(1)B组实验不变蓝的原因是淀粉被唾液淀粉酶完全分解.小柯观察到C组也不变蓝,认为氢氧化钠对酶的活性没有影响.老师提示他:“氢氧化钠会影响酶的活性.”那么,是什么原因导致C组没变蓝?小柯进一步分析并做出猜想.
猜想一:氢氧化钠变质.
猜想二:氢氧化钠与碘发生了化学反应.
…
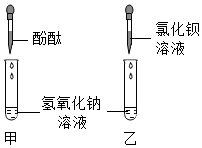
(2)小柯按图甲实验,看到溶液变红,认为氢氧化钠没有变质.小常认为他的结论是错误的,理由是变质产生的碳酸钠也能使酚酞变红.
在小常的建议下,小柯按乙实验,溶液中没有沉淀产生,从而排除了猜想一.
(3)在原来C组实验基础上,只要继续滴加碘液直到出现蓝色(写出操作和现象),就可以证明猜想二正确.
 小柯探究pH对唾液淀粉酶活性的影响,其实验过程及结果如下:
小柯探究pH对唾液淀粉酶活性的影响,其实验过程及结果如下:| 组别 | A | B | C |
| 试管中依次 加入物质 | 1ml唾液 | 1ml唾液 | 1ml唾液 |
| 1ml盐酸溶液 | 1ml蒸馏水 | 1ml氢氧化钠溶液 | |
| 2ml淀粉溶液 | 2ml淀粉溶液 | 2ml淀粉溶液 | |
| 水浴10分钟 | 37℃ | 37℃ | 37℃ |
| 各滴入2滴 碘液后的现象 | 变蓝 | 不变蓝 | 不变蓝 |
猜想一:氢氧化钠变质.
猜想二:氢氧化钠与碘发生了化学反应.
…
(2)小柯按图甲实验,看到溶液变红,认为氢氧化钠没有变质.小常认为他的结论是错误的,理由是变质产生的碳酸钠也能使酚酞变红.
在小常的建议下,小柯按乙实验,溶液中没有沉淀产生,从而排除了猜想一.
(3)在原来C组实验基础上,只要继续滴加碘液直到出现蓝色(写出操作和现象),就可以证明猜想二正确.