题目内容
向一定量硝酸银和硝酸铜的混合溶液中加入锌粉,所得溶液的质量与加入锌粉的质量关系如图所示。下列说法正确的是( )
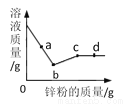
A. a点所得溶液中的溶质是硝酸铜、硝酸锌
B. 向b点所得固体中加入盐酸有气泡产生
C. c点所得固体为银和铜
D. d点所得溶液中溶质一定有硝酸锌,可能有硝酸铜
C 【解析】A、a点是锌和部分硝酸银反应,溶液中的溶质有:反应生成的硝酸锌、剩余的硝酸银和没有反应的硝酸铜,错误;B、b点时锌和硝酸银恰好反应,固体中只有银一种物质,加入盐酸没有气泡产生,错误;C、b~c段是锌和硝酸铜反应,c点表示锌和硝酸铜恰好反应,所得固体为银和铜,正确;D、d点表示锌过量,所得溶液中溶质只有硝酸锌,错误。故选C。
练习册系列答案
相关题目
为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液于试管中,用 下表中的不同试剂进行实验。以下选项正确的是
选项 | 所用试剂 | 现象和结论 |
A | 无色酚酞溶液 | 溶液不变色,则恰好完全反应 |
B | 氯化钡溶液 | 出现白色沉淀,则硫酸过量 |
C | 铜片 | 无气泡产生,则恰好完全反应 |
D | 硫酸铜溶液 | 出现蓝色沉淀,则氢氧化钠过量 |
A. A B. B C. C D. D
D 【解析】A、硫酸与氢氧化钠恰好完全反应生成硫酸钠和水,硫酸钠呈中性,不能使酚酞试液变色;但若硫酸过量,溶液呈现酸性,也不能使酚酞试液变色,错误;B、当硫酸不过量时,硫酸与氢氧化钠反应生成的硫酸钠也会和氯化钡反应生成硫酸钡白色沉淀,错误;C、铜片既不能与硫酸反应,也不能与氢氧化钠反应,铜不能检验硫酸、氢氧化钠的存在,铜片不能检验氢氧化钠溶液与稀硫酸是否恰好完全反应,错误;D、只有氢氧化钠过...


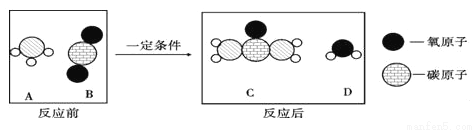
 可表示___________,
可表示___________, 的化学式为________。
的化学式为________。