题目内容
11.锂广泛应用于电池、贮氢等领域,锂在化合物中显+1价.图A是锂元素在周期表中的一些信息.图B~E是四种粒子的结构示意图,图F是一种粒子模型.
(1)从图A可获得锂元素的相对原子质量为6.941.
(2)B、C、D、E中,属于同种元素的是DE(填字母序号).
(3)F所表示物质的化学式为NH3,其中氮元素的化合价为-3价.
分析 (1)根据元素周期表的信息来分析;
(2)依据质子数不同元素种类不同分析解答;
(3)根据分子结构模型来书写化学式,结合化学式来分析化合价.
解答 解:(1)由元素周期表可知,锂元素的相对原子质量为6.941;故填:6.941;
(2)D和E核内质子数相同,属于同种元素;故填:DE;
(3)由分子结构模型可知,一个该分子是由1个氮原子和3个氢原子构成的,所以其化学式为NH3,其中氢元素显+1价,设氮元素的化合价为x,由化合物中各元素化合价的代数和为零原则可知,x+(+1)×3=0,x=-3;故填:NH3;-3.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、化合价原则以及化学用语进行分析解题的能力.

练习册系列答案
相关题目
6.下列有关事故的处理方法正确的是( )
| A. | 发现屋内煤气泄漏时,立即打开排气扇 | |
| B. | 皮肤不慎沾到浓硫酸时,立即涂NaOH溶液 | |
| C. | 炒菜油锅着火时,立即用锅盖盖灭 | |
| D. | 高层住房着火时,立即打开所有门窗 |
20.下列说法中错误的是( )
| A. | 月饼盒中放入装有铁粉的小包装,可以防止月饼变质 | |
| B. | 液化气泄漏时,应首先关闭阀门,打开门窗换气 | |
| C. | 车船表面喷涂油漆,可防止生锈 | |
| D. | 石油、天然气、甲烷是三大重要的化石燃料 |
1.如图是甲、乙两物质的溶解度曲线(不含结晶水),下列说法正确的是( )


| A. | 甲的溶解度大于乙的溶解度 | |
| B. | 乙的不饱和溶液降温可变为饱和溶液 | |
| C. | 20℃,甲乙两物质的溶解度相等 | |
| D. | 50℃,甲的饱和溶液溶质质量分数为40% |

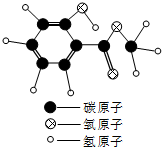 复方冬青软膏具有强力迅速镇痛作用,其有效成分A的分子模型如图所示.
复方冬青软膏具有强力迅速镇痛作用,其有效成分A的分子模型如图所示.