题目内容
金属不仅其物理性能优良,还与化学性质密切相关.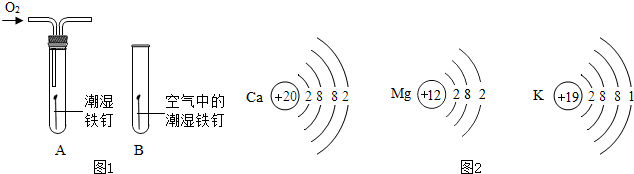
(1)钛被称为“21世纪金属”,呈灰色,能在氮气中燃烧,熔点高.钛和钛合金是新型的结构材料,主要用于航天和航海工业.上述描述中属于钛化学性质的是 .
(2)某小组用图1所示装置对铁生锈的条件进行探究.4min后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是 .
(3)工业生产常用的稀盐酸来除铁锈( Fe2O3),写出除锈的化学方程式 .实验室用浓盐酸配制10%稀盐酸时,用到的主要仪器有烧杯、量筒、玻璃棒,那么玻璃棒的作用是 .
(4)在金属活动顺序表中,金属位置越靠前,越容易失去电子.Ca、Mg、K三种金属失电子能力由强到弱的顺序是 ,如图2是三种原子的结构示意图,据此推测金属失电子能力的强弱除与最外层电子数有关外,还可能与 有关.

(1)钛被称为“21世纪金属”,呈灰色,能在氮气中燃烧,熔点高.钛和钛合金是新型的结构材料,主要用于航天和航海工业.上述描述中属于钛化学性质的是
(2)某小组用图1所示装置对铁生锈的条件进行探究.4min后发现A中铁钉表面灰暗,B中铁钉依然光亮,对比A、B现象说明:决定铁生锈快慢的一个重要因素是
(3)工业生产常用的稀盐酸来除铁锈( Fe2O3),写出除锈的化学方程式
(4)在金属活动顺序表中,金属位置越靠前,越容易失去电子.Ca、Mg、K三种金属失电子能力由强到弱的顺序是
考点:金属的化学性质,一定溶质质量分数的溶液的配制,金属活动性顺序及其应用,金属锈蚀的条件及其防护,酸的化学性质,原子结构示意图与离子结构示意图
专题:金属与金属材料
分析:(1)物质在化学变化中表现出来的性质叫做物质的化学性质;
(2)铁生锈的条件是铁与氧气、水共同作用的结果,对比A、B两图,就是空气与氧气的差别;
(3)铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水;配制溶液所需要的仪器主要有量筒、烧杯、玻璃棒、胶头滴管;
(4)熟记金属活动性顺序才能解决此题.
(2)铁生锈的条件是铁与氧气、水共同作用的结果,对比A、B两图,就是空气与氧气的差别;
(3)铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水;配制溶液所需要的仪器主要有量筒、烧杯、玻璃棒、胶头滴管;
(4)熟记金属活动性顺序才能解决此题.
解答:解:
(1)物质在化学变化中表现出来的性质叫做物质的化学性质,例如可燃性、还原性等,故答案为:能在氮气中燃烧;
(2)铁生绣的条件是铁与氧气、水共同作用的结果,对比A、B两图,就是空气与氧气的差别,故答案为:氧气的浓度;
(3)铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水,其化学方程式为Fe2O3+6HCl=2FeCl3+3H2O;配制溶液所需要的仪器主要有量筒、烧杯、玻璃棒、胶头滴管,其中玻璃棒的作用是搅拌.
(4)根据所学的金属活动性顺序和题目的已知条件“在金属活动顺序表中,金属位置越靠前,越容易失去电子”,可知Ca、Mg、K三种金属失去电子能力由强到弱的顺序是K、Ca、Mg;根据题目所给的原子结构示意图,发现Mg比K、Ca少一个电子层.故答案为:K、Ca、Mg;电子层数.
故答案为:
(1)能在氮气中燃烧.
(2)氧气的浓度.
(3)Fe2O3+6HCl=2FeCl3+3H2O. 搅拌.
(4)K、Ca、Mg,电子层数.
(1)物质在化学变化中表现出来的性质叫做物质的化学性质,例如可燃性、还原性等,故答案为:能在氮气中燃烧;
(2)铁生绣的条件是铁与氧气、水共同作用的结果,对比A、B两图,就是空气与氧气的差别,故答案为:氧气的浓度;
(3)铁锈的主要成分是氧化铁,它能与稀盐酸反应生成氯化铁和水,其化学方程式为Fe2O3+6HCl=2FeCl3+3H2O;配制溶液所需要的仪器主要有量筒、烧杯、玻璃棒、胶头滴管,其中玻璃棒的作用是搅拌.
(4)根据所学的金属活动性顺序和题目的已知条件“在金属活动顺序表中,金属位置越靠前,越容易失去电子”,可知Ca、Mg、K三种金属失去电子能力由强到弱的顺序是K、Ca、Mg;根据题目所给的原子结构示意图,发现Mg比K、Ca少一个电子层.故答案为:K、Ca、Mg;电子层数.
故答案为:
(1)能在氮气中燃烧.
(2)氧气的浓度.
(3)Fe2O3+6HCl=2FeCl3+3H2O. 搅拌.
(4)K、Ca、Mg,电子层数.
点评:此题综合考查学生对金属有关知识的掌握程度,提高分析和解决实际问题的能力,是中考考试的热点.

练习册系列答案
相关题目
下列做法与社会可持续发展理念相违背的是( )
| A、将工业废水注入地下,治理水污染 |
| B、采用化石燃料除硫技术 |
| C、开发新能源,代替化石燃料 |
| D、推行自行车、公交车等出行方式,减少“碳”排放 |
爱护水资源人人有责.下列日常生活行为不利于保护水资源的是( )
| A、加大施用农药、化肥力度以提高蔬菜产量,满足日常生活需要 |
| B、少用或不用含磷洗衣粉可有效防止水体富营养化 |
| C、在灌溉农田、草坪时,应大力提倡滴灌或喷灌 |
| D、将工业用水沉降、过滤后再利用,虽然成本高,但也值得提倡 |
 五常大米全国闻名,用大米做出的米饭是人们喜欢吃的主食,米饭所提供的营养素对生命活动的主要作用是
五常大米全国闻名,用大米做出的米饭是人们喜欢吃的主食,米饭所提供的营养素对生命活动的主要作用是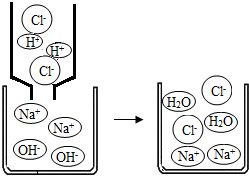 氢氧化钠和稀盐酸能够发生中和反应.
氢氧化钠和稀盐酸能够发生中和反应.