��Ŀ����
��п��������п������п��������Ҫ����;
I.�Ժ�п��������Ҫ�ɷ�ΪZnO,����ΪFeO�pCuO��Ϊԭ���Ʊ���ˮ����п��ZnSO4��7H2O�����������¡�

�ŷ����Ŀ���� ��
����ʵ��������������Ϊ98%����������200g25%�����ᣬ��Ҫ�IJ��������н�ͷ�ιܩp�������p �� ���˴��������������� ��
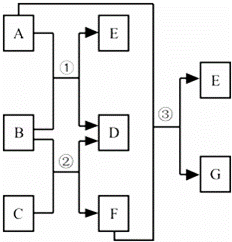
������X�� �������к��еĽ��������� ����ͭʱ�����ķ�Ӧ���� ��Ӧ���������Ӧ���ͣ�
�������л����ˮ����пǰʡ�ԵIJ����� �p��ȴ�ᾧ�p ϴ�Ӻ͵��º�ɡ�
��ij�¶��£�Fe(OH)3�ֽ�õ�һ�����p��������21:8���������������Ļ�ѧʽ ��
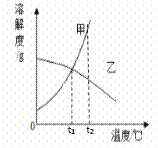
�ʳ��������У��¶�pH�Գ���Ч����Ӱ��ֱ����ͼ��ʾ����ͼ��֪������ʱ�¶�Ӧ������ ��Ϊ�ˣ�pHӦ������ Ϊ�ˡ�

II.��ij��п��ZnCO3����Ϊ62.5%��Ϊԭ���Ʊ�п��ԭ�����£��������ʲ��μӷ�Ӧ����
 ��100����������п������������Ƶ�п���ٶ֣���д��������̣�
��100����������п������������Ƶ�п���ٶ֣���д��������̣�
���㣺I.���ʵ��Ʊ���ת����Ũ����ϡ��ϡ������ʵĹ��ˣ����ʵij��ӣ��û���Ӧ�������غ㶨�ɵ�Ӧ��II���ݻ�ѧ��Ӧ����ʽ�ļ��㡣
�������Ź���ı����Խ��ѧ��Ӧ����Խ�졣��п���������Ŀ��������Ӵ�������ӿ췴Ӧ���ʣ���ַ�Ӧ��
��Ũ����ϡ�����������õ�����Ͳ���ιܡ�ϸ��ƿ�����������ձ���ͨ���ȽϿ�֪����ȱ���ձ�����Ͳ���˴��������������ǽ��裬��������ʱ����ɢ��
�Ǽ��������X��Ŀ���dz�ȥͭ����С��ʵ�������ʵij��ӣ���Ҫ��ȥ������Ҫ���������µ����ʣ����ǵ��������˳��X������п����������п���û���ͭ�������Ӧ�������û���Ӧ��
�����Ƿ�������Թ����Һ��ķ������Ƚ��ȵı�����Һ��ȴ������ͻ������������о��������ı�����Һ�����ˣ���������ˮϴ�ӣ��ٵ��º�ɡ����Բ����IJ����ǣ�����Ũ������ȴ�ᾧ�����ˣ�ϴ�Ӻ͵��º��
��Fe(OH)3�ֽ�õ�һ�����p��������21:8����������������������֣�Fe2O3,FeO, Fe3O4.�Ƚ�������������21:8ֻ��Fe3O4�������⡣
�ʹؼ���������ͼ��X���Y������ĺ��壬Ϊ�˳���Ч����ѣ�������Ҫ�ҳ���߳����ʶ�Ӧ���¶Ⱥ�pH.
II.��ĿҪ���������������Ƶ�п���ٶ�
��������������Ƶ�п������ΪX��
���������֪ZnCO3��������=100t��62.5%=62.5t

 ����������ʽ��֪��
����������ʽ��֪��
ZnCO3 ~ Zn
125 65
62.5t X 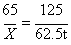 x=32.5t
x=32.5t

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�