题目内容

 硝酸铜为蓝色固体,溶于水可得蓝色溶液。某实验小组同学用右图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃。
硝酸铜为蓝色固体,溶于水可得蓝色溶液。某实验小组同学用右图装置加热硝酸铜,发现固体由蓝色逐渐变黑,同时产生红棕色有刺激性气味的气体,带火星的木条复燃。
【提出问题】硝酸铜在加热条件下到底发生了怎样的反应?
|
①  氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4
氧化铜和稀硫酸反应的化学方程式:CuO+H2SO4  CuSO4+H2O
CuSO4+H2O
② 含氮化合物中,只有NO2是红棕色、有刺激性气味的气体。
③ NO2有助燃性,能使带火星的木条复燃
【猜想假设】
Cu(NO3)2受热分解除了生成_______,还可能生成了CuO和O2。
【进行实验】
| 实验操作 | 实验现象 | 实验结论 |
| 步骤I:将反应后试管中的固体加水充分溶解, ① ,加热 | 固体全部溶解,得到蓝色溶液 | 硝酸铜分解生成了氧化铜。 |
|
| 集气瓶中气体为无色,带火星木条复燃 | 硝酸铜分解生成了氧气 |
步骤II是同学们查阅了新的资料后设计完成的。该资料是关于NO2___②__方面的性质信息。
【获得结论】 根据实验结果,Cu(NO3)2受热分解的化学方程式为_______。
【反思与评价】
已知相同状况下,气体的体积比等于其分子个数比。据此,同学们认为,即使没有资料③,依据实验结论和“加热硝酸铜产生的气体能 使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性。理由是______。
使带火星的木条复燃”的实验现象,也能推出NO2可能具有助燃性。理由是______。
[猜想假设] NO2[进行实验]①过滤,洗涤,向滤渣中加入足量稀硫酸
②NO2的沸点(或低温下NO2能否反应生成液态或固态物质)
[获得结论] 2Cu(NO3)2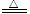 2CuO+4NO2↑+ O2↑
2CuO+4NO2↑+ O2↑
[分析及反思]硝酸铜分解生成的气体中NO2与O2的体积比为4:1,O2所占的体积分数与空气中O2的体积分数相同,分解生成气体能使带火星木条复燃而空气不能,说明NO2有助燃性(此空2分,、、
答对任意一处即给1分,三处答全给2分)

 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案一个密闭容器中加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,测得数据见表.下列说法中正确的是( )
A. x=9g  B.该反应是化合反应
B.该反应是化合反应
C. 该反应中,丙物质一定做催化剂 
D.在该反应的化学方程式中,丙、丁的化学计量数比为1:1
| 物质质量 | 田 | 乙 | 丙 | 丁 |
| 反应前 | 25g | x | 5g | 5g |
| 反应后 | 8g | 23g | 5g | 8g |
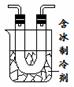 步骤II:在图1的
步骤II:在图1的




