题目内容
13.12.5g碳酸钙高温煅烧一段时间后,剩余8.1g固体,计算:(1)生成二氧化碳的质量.
(2)分解的碳酸钙的质量.
(3)剩余固体中钙元素的质量分数(计算结果保留到1%).
分析 碳酸钙在高温条件下分解生成氧化钙和二氧化碳,反应前后的质量差即为反应生成二氧化碳的质量,根据二氧化碳的质量可以计算碳酸钙的质量;
12.5g碳酸钙中钙元素的质量即为剩余固体中钙元素的质量,进一步可以计算剩余固体中钙元素的质量分数.
解答 解:(1)生成二氧化碳的质量为:12.5g-8.1g=4.4g,
(2)设:分解的碳酸钙的质量为x,
CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,
100 44
x 4.4 g
$\frac{100}{x}$=$\frac{44}{4.4g}$,
x=10g,
(3)碳酸钙中钙元素的质量为:12.5g×$\frac{40}{100}$×100%=5g,
剩余固体中钙元素的质量分数为:$\frac{5g}{8.1g}$×100%=62%,
答:生成二氧化碳的质量是4.4g,分解的碳酸钙为10g,剩余固体中钙元素的质量分数为62%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.下列关于溶液的说法正确的是( )
| A. | 氯化亚铁溶液是浅绿色的 | |
| B. | 汽油洗油污是利用了乳化原理 | |
| C. | 升高温度既能加快溶解速率又能增大溶解度 | |
| D. | 溶液中溶质只有一种 |
8.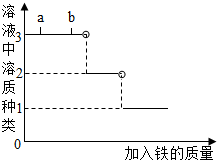 某溶液中含有Cu(NO3)2和AgNO3,向其中逐渐加入一定质量的铁粉进行处理,并绘制加入铁的质量与溶液中溶质种类的关系图.下列说法正确的是( )
某溶液中含有Cu(NO3)2和AgNO3,向其中逐渐加入一定质量的铁粉进行处理,并绘制加入铁的质量与溶液中溶质种类的关系图.下列说法正确的是( )
 某溶液中含有Cu(NO3)2和AgNO3,向其中逐渐加入一定质量的铁粉进行处理,并绘制加入铁的质量与溶液中溶质种类的关系图.下列说法正确的是( )
某溶液中含有Cu(NO3)2和AgNO3,向其中逐渐加入一定质量的铁粉进行处理,并绘制加入铁的质量与溶液中溶质种类的关系图.下列说法正确的是( )| A. | a、b两点,溶液的质量相等 | |
| B. | 当溶质种类为1种时,金属单质种类可能为1种 | |
| C. | 当溶质种类为2种时,金属单质种类可能为2种 | |
| D. | 当溶质种类为3种时,金属单质的种类也为3种 |
18.“善存”片富含维生素及钾和镁等,钾和镁指的是( )
| A. | 分子 | B. | 原子 | C. | 离子 | D. | 元素 |
5.下列物质放入水中,能形成溶液的是( )
| A. | 碳酸钙 | B. | 蔗糖 | C. | 花生油 | D. | 面粉 |
2.下列关于相应微粒的描述中,正确的是( )
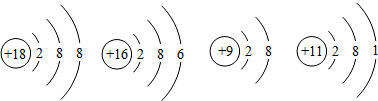
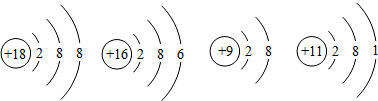
| A. | 化学性质活泼 | B. | 易形成阳离子 | C. | 带负电荷 | D. | 易得电子 |