题目内容
镁是一种化学性质比较活泼的金属,在空气中能剧烈燃烧,点燃后能在氮气和二氧化碳中剧烈燃烧。已知镁在氮气中燃烧化合成一种物质,其中氮元素的化合价是-3价;镁在二氧化碳中燃烧生成一种金属氧化物和一种黑色非金属单质。试写出镁在空气中燃烧可能发生反应的化学方程式:
(1) ;
(2) ;
(3) 。
(1)2Mg + O2 点燃 2MgO (2)3Mg + N2 点燃 Mg3N2 (3)2Mg + CO2 点燃 2MgO+C

根据下图四个化学实验,回答问题:(提示:Cu与Zn的合金称为黄铜)
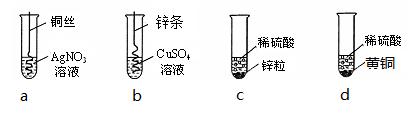
①描述实验a中的实验现象 (12) 。
②要证明Cu、Zn、Ag的活动性顺序,必须要做的实验是 (13) (填实验序号)。
③在c实验后的剩余溶液中,一定有的溶质是 (14) ,可能有的溶 质是 (15) ,为了确定可能有的溶质,可加入 (16) (填选项序号)
质是 (15) ,为了确定可能有的溶质,可加入 (16) (填选项序号)
Ⅰ.氯化钡溶液 Ⅱ.氢氧化铜 Ⅲ.氢氧化钠溶液 Ⅳ.锌粒
④为了测定d中稀硫酸的溶质质量分数,取20g该黄铜样品于烧杯中,向其中分4次加入该稀硫酸,充分反应。每次所用稀硫酸的质量及剩余固体的质量记录于下表:
| 加入稀硫酸的质量(g) | 充分反应后剩余固体的质量(g) | |
| 第1次 | 25 | 16.75 |
| 第2次 | 25 | 13.5 |
| 第3次 | 25 | m |
| 第4次 | 2 | 12.0 |
试回答下列问题:
Ⅰ.上述表格中m的值为 (17) ;
Ⅱ.该稀硫酸的溶质质量分数是多少?(根据化学方程式计算)
 反应,生成44份质量的二氧化碳
反应,生成44份质量的二氧化碳 5
5 ,不溶于水;碳酸氢钠是白色固体,溶于水。碳酸氢钠受热易分解,反应方程式为
,不溶于水;碳酸氢钠是白色固体,溶于水。碳酸氢钠受热易分解,反应方程式为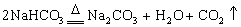 。
。