题目内容
1.清明节假期,小明同学去瑞昌市的赤湖边郊游.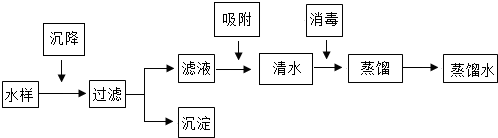
(1)在沉降步骤中,可以加一种絮凝剂,最常见的絮凝剂是明矾;
(2)在吸附步骤中,可以加入活性炭,除去水样中的色素和异味;
(3)上述实验中的“水”,属于纯净物的有C(填字母);
A、水样 B、清水 C、蒸馏水
(4)检验湖水是硬水还是软水的方法是肥皂水;
(5)自来水常用氯气消毒,反应原理为Cl2+H2O═HClO+X,则X的化学式为HCl;
(6)在自制蒸馏水的过程中,在水中要放碎瓷片,其作用是防止加热时出现暴沸.
分析 (1)根据明矾可以吸附较大颗粒,加速沉降进行解答;
(2)根据活性炭具有吸附作用,能够吸附水中的色素和异味进行解答;
(3)根据纯净物由一种物质组成,混合物由两种或两种以上的物质组成解答;
(4)根据用肥皂水区分地下水是软水还是硬水进行解答;
(5)根据质量守恒定律可知反应前后各种原子的种类和数目不变求出化学式;
(5)根据碎瓷片能够防止液体暴沸进行解答.
解答 解:(1)在沉降步骤中,可以加一种絮凝剂,最常见的絮凝剂是明矾,明矾可以吸附较大颗粒,加速沉降;
(2)活性炭具有吸附作用,能够吸附水中的色素和异味;故填:活性炭;
(3)水样 和清水中含有水和一些溶于水的物质,属于混合物. 蒸馏水是由一种物质组成的,属于纯净物;
(4)肥皂水区分地下水是软水还是硬水,泡沫多的是软水,泡沫少的是硬水;故填:肥皂水;
(5)由Cl2+H2O=X十HClO可知反应物中含有2个氯原子、2个氢原子、1个氧原子,生成物中含有1个氢原子、1个氯原子、1个氧原子,所以还少1个氢原子、1个氯原子,所以X的化学式是:HCl;
故答案为:HCl;
(6)在制取蒸馏水的过程中,在水中要放碎瓷片,其作用是防止加热时出现暴沸;
答案:
(1)明矾;
(2)活性炭;
(3)C;
(4)肥皂水;
(5)HCl;
(6)防止加热时出现暴沸.
点评 熟练掌握净化水的方法,要充分理解明矾、活性炭的性质及它们的作用,并能熟练的运用.混合物中至少含有两种物质,根据组成物质的种类就可以判断该物质属于混合物,还是属于纯净物.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
11.在一次化学实验中,同学们将饱和CuSO4溶液逐滴加到5mL饱和NaOH溶液中,观察到以下异常实验现象:
在实验①中同学们根据所学初中化学知识判断蓝色沉淀是Cu(OH)2,请你写出生成蓝色沉淀的化学方程式CuSO4+2NaOH=Cu(OH)2↓+Na2SO4.
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】Ⅰ.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO.
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解.其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体.
同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中.
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色.
【实验探究】
为验证猜想,同学们用Cu(OH)2粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
【结论与反思】
(1)根据实验,并进一步查阅资料知道,Cu(OH)2在NaOH溶液中溶解并生成Na2Cu(OH)4,反应的化学方程式是Cu(OH)2+2NaOH=Na2Cu(OH)4.
(2)根据实验可知,饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色.
(3)若同学们将药品的加入顺序改为把饱和NaOH溶液逐滴加到5mL饱和CuSO4溶液中,将出现的现象是蓝色固体开始不消失;随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色.
| 实验序号 | 滴加CuSO4溶液的量 | 实验现象 |
| ① | 第1-6滴 | 产生蓝色沉淀,但振荡后沉淀消失,形成亮蓝色溶液 |
| ② | 第7-9滴 | 产生蓝色沉淀,且沉淀逐渐增多,振荡后沉淀不消失,快沉淀逐渐变黑色 |
实验①中蓝色沉淀为什么消失?同学们继续进行如下探究.
【查阅资料】Ⅰ.Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO.
Ⅱ.酮酸钠[Na2Cu(OH)4]溶于水,溶液呈亮蓝色.
【猜想与讨论】小陶认为蓝色沉淀消失可能是Cu(OH)2发生了分解.其他同学一致否定了他的猜测,理由是沉淀消失,形成亮蓝色溶液,而氢氧化铜分解产生的是黑色固体.
同学们交流讨论后,提出以下两种猜想.
猜想一:少许Cu(OH)2可溶于足量水中.
猜想二:Cu(OH)2可在足量NaOH浓溶液中溶解,溶液呈亮蓝色.
【实验探究】
为验证猜想,同学们用Cu(OH)2粉末(其它试剂可任选)设计如下实验.请你填写表中的空格.
| 实验序号 | 实验方法与操作 | 实验现象 | 结论 |
| ③ | 将少许Cu(OH)2粉末加到5mL蒸馏水中,充分振荡 | 沉淀不消失 | 猜想一 错误 |
| ④ | 将少许Cu(OH)2粉末加到NaOH浓溶液中,充分振荡 | 沉淀消失,溶液变成亮蓝色 | 猜想二 正确 |
(1)根据实验,并进一步查阅资料知道,Cu(OH)2在NaOH溶液中溶解并生成Na2Cu(OH)4,反应的化学方程式是Cu(OH)2+2NaOH=Na2Cu(OH)4.
(2)根据实验可知,饱和CuSO4溶液与饱和NaOH溶液的反应是放热反应,依据的实验现象是资料Ⅰ显示Cu(OH)2在室温下稳定,70℃-80℃时可脱水分解生成CuO,而表格1可知随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色.
(3)若同学们将药品的加入顺序改为把饱和NaOH溶液逐滴加到5mL饱和CuSO4溶液中,将出现的现象是蓝色固体开始不消失;随着氢氧化钠溶液的滴加,观察到产生蓝色沉淀,且沉淀逐渐增多.振荡后沉淀不消失,很快沉淀逐渐变黑色.
9.2016年3月22日,相关媒体报道:山东警方破获案值5.7亿元非法疫苗案,经食药监管部门核查,疫苗虽为正规厂家生产但由于相关人员未按照国家相关法律规定运输、保存,使疫苗脱离了2-8℃的恒温冷链,难以保证其品质和使用效果.下列与疫苗相关的叙述中一定涉及化学变化的是( )
| A. | 按要求保存疫苗 | B. | 用正确方法运输疫苗 | ||
| C. | 用注射器吸取疫苗 | D. | 疫苗变质失效 |
16. 某同学用如图所示装置探究可燃物燃烧的条件,得到以下实验现象:①烧杯中的白磷不燃烧;②铜片上的红磷不燃烧;③铜片上的白磷燃烧.能证明可燃物必须与氧气接触才能燃烧的实验现象是( )
某同学用如图所示装置探究可燃物燃烧的条件,得到以下实验现象:①烧杯中的白磷不燃烧;②铜片上的红磷不燃烧;③铜片上的白磷燃烧.能证明可燃物必须与氧气接触才能燃烧的实验现象是( )
 某同学用如图所示装置探究可燃物燃烧的条件,得到以下实验现象:①烧杯中的白磷不燃烧;②铜片上的红磷不燃烧;③铜片上的白磷燃烧.能证明可燃物必须与氧气接触才能燃烧的实验现象是( )
某同学用如图所示装置探究可燃物燃烧的条件,得到以下实验现象:①烧杯中的白磷不燃烧;②铜片上的红磷不燃烧;③铜片上的白磷燃烧.能证明可燃物必须与氧气接触才能燃烧的实验现象是( )| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |
6.鸡蛋壳的主要成分是碳酸钙.为了测定某鸡蛋壳中碳酸钙的质量分数,兴趣小组的同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取20g放在烧杯里,然后分4次向烧杯中加入等质量稀盐酸,实验数据如表所示(假设其他物质捕鱼盐酸反应):
根据实验数据回答问题:
(1)表中数据值M=213.4;
(2)完全反应后产生二氧化碳的质量为6.6;
(3)计算该鸡蛋壳中碳酸钙的质量分数(写出计算过程).
| 数据 | 实验1 | 实验2 | 实验3 | 实验4 | 实验5 |
| 加入稀盐酸的质量/g | 0 | 50 | 50 | 50 | 50 |
| 烧杯与烧杯中物质的总质量/g | 70.00 | 117.5 | 165.0 | M | 263.4 |
(1)表中数据值M=213.4;
(2)完全反应后产生二氧化碳的质量为6.6;
(3)计算该鸡蛋壳中碳酸钙的质量分数(写出计算过程).
13.今年“世界水日”的宣传主题是“水与能源”.以下对水的利用过程中主要发生化学变化的是( )
| A. | 水力发电 | B. | 用水灭火 | C. | 水溶解糖 | D. | 水的电解 |