题目内容
10.将一块质量为20.5g的黄铜片(假设仅含铜、锌)与足量的稀盐酸恰好完全反应后,得到0.2g氢气.求:(1)所得溶液中溶质的质量.
(2)黄铜片中铜的质量.
分析 锌和稀盐酸反应生成氯化锌和氢气,根据氢气质量可以计算锌的质量和反应生成氯化锌的质量,进一步可以计算黄铜片中铜的质量.
解答 解:(1)设锌质量为x,生成氯化锌质量为y,
Zn+2HCl═ZnCl2+H2↑,
65 136 2
x y 0.2g
$\frac{65}{x}$=$\frac{136}{y}$=$\frac{2}{0.2g}$,
x=6.5g,y=13.6g,
答:所得溶液中溶质氯化锌的质量是13.6g.
(2)黄铜片中铜的质量为:20.5g-6.5g=14g,
答:黄铜片中铜的质量为14g.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
20.下列变化属于物理变化的是( )
| A. | CO使人中毒 | |
| B. | 澄清石灰水长期露置在空气中 | |
| C. | 二氧化碳的水溶液使紫色石蕊试液变红 | |
| D. | 干冰变为二氧化碳气体 |
1.密闭容器内有a、b、c、d四种物质,在一定条件下充分反应,测得反应前后各物质的质M如表.
(1)分析表中数据可知,待测数据的值为13;该反应中可能是催化剂的物质是c.
(2)该反应的反应物有两种,该反应中a与b之间反应的质量比为1:5.
| 物质 | a | b | c | d |
| 反应前物质质量/g | 18 | 1 | 2 | 32 |
| 反应后物质质量/g | 待测 | 26 | 2 | 12 |
(2)该反应的反应物有两种,该反应中a与b之间反应的质量比为1:5.
18.王萌同学想在实验室中探究某物质溶解时的吸热或放热现象,于是她进行了下列操作:她先测量烧杯中水的温度,温度计的示数为20℃,然后她向烧杯中加入该种物质并待其完全溶解后,测得烧怀内溶液的温度为10℃.则她加入的物质可能是( )
| A. | 蔗糖 | B. | 氢氧化钠 | C. | 硝酸铵 | D. | 食盐 |
3.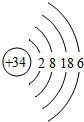 硒(Se)是人体必需的微量元素,它可以有效的调节人体的免疫功能,迅速增加人体的抵抗能力,有延缓衰老的神奇作用.已知硒原子的相对原子质量为80,其原子结构示意图如图所示,则下列说法中正确的是( )
硒(Se)是人体必需的微量元素,它可以有效的调节人体的免疫功能,迅速增加人体的抵抗能力,有延缓衰老的神奇作用.已知硒原子的相对原子质量为80,其原子结构示意图如图所示,则下列说法中正确的是( )
 硒(Se)是人体必需的微量元素,它可以有效的调节人体的免疫功能,迅速增加人体的抵抗能力,有延缓衰老的神奇作用.已知硒原子的相对原子质量为80,其原子结构示意图如图所示,则下列说法中正确的是( )
硒(Se)是人体必需的微量元素,它可以有效的调节人体的免疫功能,迅速增加人体的抵抗能力,有延缓衰老的神奇作用.已知硒原子的相对原子质量为80,其原子结构示意图如图所示,则下列说法中正确的是( )| A. | 硒元素在元素周期表中位于第四周期第六主族元素 | |
| B. | 在Na2SeO3中Se的化合价为+6 | |
| C. | 硒原子的核电荷数为46 | |
| D. | 由于硒元素的神奇作用,人们应该大量补充硒元素,增强人的抵抗力 |
4.按金属氧化物、碱、盐的顺序排列的一组物质是( )
| A. | 干冰、纯碱、氯化钾 | B. | 生铁、火碱、硝酸银 | ||
| C. | 氧化汞、熟石灰、小苏打 | D. | 生石灰、烧碱、石灰石 |
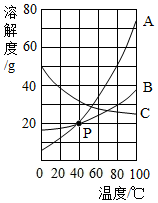 如图所示的是A、B、C三种固体物质的溶解度曲线.
如图所示的是A、B、C三种固体物质的溶解度曲线.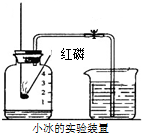 小冰同学在利用知图所示装置测量空气里氧气的含量.经检查装置气密性良好.请回答下列问题:
小冰同学在利用知图所示装置测量空气里氧气的含量.经检查装置气密性良好.请回答下列问题: