题目内容
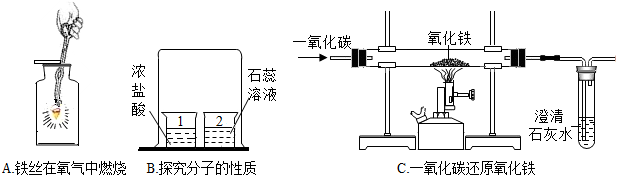
1.硫在空气中燃烧,发出淡蓝色火焰,放出热量,并生成一种有刺激性气味的气体;硫在氧气中燃烧,发出蓝紫色火焰;请写出该反应的文字表达式:硫+氧气$\stackrel{点燃}{→}$二氧化硫.分析 根据硫在空气和氧气中燃烧的现象和发生的反应分析回答.
解答 解:硫在空气中燃烧,发出淡蓝色火焰,放出热量,并生成一种有刺激性气味的气体;硫在氧气中燃烧,发出蓝紫色火焰;该反应的文字表达式是:硫+氧气$\stackrel{点燃}{→}$二氧化硫.
故答为:淡蓝,有刺激性气味,蓝紫,硫+氧气$\stackrel{点燃}{→}$二氧化硫.
点评 本题较为简单,了解硫燃烧的现象和发生的反应即可分析解答.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
12.甲、乙、丙三位同学利用下图装置,探究化学反应是否遵守质量守恒定律,请参与其中并回答相关问题:
【实验步骤】
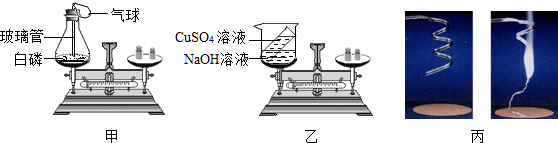
①如图所示,甲将白磷和反应装置、乙将装有硫酸铜溶液的小试管和盛有氢氧化钠溶液的烧杯,分别放在两架天平的托盘上,并用砝码使天平平衡.丙对石棉网和打磨干净的镁条进行称量.
②三位同学分别引发反应发生.
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘上,观察天平是否平衡.丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量.
【实验分析】
①请你仿照示例,完成实验现象的记录和分析.
②通过上述实验现象的对比分析,甲、乙两位同学发现丙同学的实现现象是正确的,但是结论是错误的.在实验操作完全正确的情况下,请分析导致丙同学实验前后质量不相等的原因是反应前未称量参加反应的氧气的质量,反应后部分生成的氧化镁外逸,也无法称量.
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】请从微观角度分析化学反应遵守质量守恒定律的原因是化学反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变..

【实验步骤】
①如图所示,甲将白磷和反应装置、乙将装有硫酸铜溶液的小试管和盛有氢氧化钠溶液的烧杯,分别放在两架天平的托盘上,并用砝码使天平平衡.丙对石棉网和打磨干净的镁条进行称量.
②三位同学分别引发反应发生.
③甲、乙同学在反应结束且甲的装置冷却后,将反应装置及装置内的物质放在反应前使用的托盘上,观察天平是否平衡.丙同学实验结束后称量石棉网和石棉网上氧化镁的质量,比较反应前后质量.
【实验分析】
①请你仿照示例,完成实验现象的记录和分析.
| 实验现象 | 化学方程式 | 结论 | |
| 甲 | 白磷燃烧产生大量白烟 放热,气球先膨胀后变小 | □P+□O2$\frac{\underline{\;点燃\;}}{\;}$□P2O5 (配平该反应方程式) | 该反应遵守质量守恒定律 |
| 乙 | 混合后有蓝色沉淀产生 | 2NaOH+CuSO4═Na2SO4+Cu(OH)2↓ | 该反应遵守质量守恒定律 |
| 丙 | 镁条剧烈燃烧,发出耀眼白光,放热,生成白色固体.反应前后称量质量不相等. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | 该反应不遵守质量守恒定律 |
【实验结论】化学反应都遵守质量守恒定律.
【实验反思】请从微观角度分析化学反应遵守质量守恒定律的原因是化学反应前后原子的种类没有改变,数目没有增减,原子的质量也没有改变..
9. 在一个堆放了一批袋装化肥(主要成分为碳酸氢铵)的小仓库里,过了一个夏天,管理员发现仓库里这种化肥所特有的刺激性气味变得浓烈了,有些袋里的化肥变少了.检查发现,变少的化肥包装袋有少许破损,但没有发现化肥落在地上.
在一个堆放了一批袋装化肥(主要成分为碳酸氢铵)的小仓库里,过了一个夏天,管理员发现仓库里这种化肥所特有的刺激性气味变得浓烈了,有些袋里的化肥变少了.检查发现,变少的化肥包装袋有少许破损,但没有发现化肥落在地上.
(1)你认为袋中化肥变少的原因可能是什么?请与同学讨论,提出相应的假设.
(2)根据上述信息,你是否能证实(或否定)你或其他同学所提出的假设?
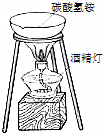
(3)观察如图的实验,记录实验现象,通过联想、推理,你能确定这些化肥消失的原因吗?你认为在保存碳酸氢铵化肥时需要注意什么问题?请将实验结果记录在表中.
 在一个堆放了一批袋装化肥(主要成分为碳酸氢铵)的小仓库里,过了一个夏天,管理员发现仓库里这种化肥所特有的刺激性气味变得浓烈了,有些袋里的化肥变少了.检查发现,变少的化肥包装袋有少许破损,但没有发现化肥落在地上.
在一个堆放了一批袋装化肥(主要成分为碳酸氢铵)的小仓库里,过了一个夏天,管理员发现仓库里这种化肥所特有的刺激性气味变得浓烈了,有些袋里的化肥变少了.检查发现,变少的化肥包装袋有少许破损,但没有发现化肥落在地上.(1)你认为袋中化肥变少的原因可能是什么?请与同学讨论,提出相应的假设.
(2)根据上述信息,你是否能证实(或否定)你或其他同学所提出的假设?
(3)观察如图的实验,记录实验现象,通过联想、推理,你能确定这些化肥消失的原因吗?你认为在保存碳酸氢铵化肥时需要注意什么问题?请将实验结果记录在表中.
| 实验过程 | 实验现象 | 实验结论 | 碳酸氢铵保存注意点 |
| 取少量碳酸氢铵固体粉末放入蒸发皿 | 固体逐渐减少,有刺激性气味的气体产生 | 碳酸氢铵受会发生分解 | 注意密封保存、避免暴晒 |
16.下列物质溶于水后,溶液温度无明显变化的是( )
| A. | 氢氧化钠 | B. | 浓硫酸 | C. | 氯化钠 | D. | 生石灰 |
13.铁丝在氧气中燃烧的实验现象中哪个能有力地说明发生了化学反应( )
| A. | 剧烈燃烧 | B. | 放热 | C. | 火星四射 | D. | 生成黑色固体 |
11.实验是学习化学的重要途径,小亮在学习酸碱盐的化学性质时做了如下实验,请你和他一起完成实验活动.
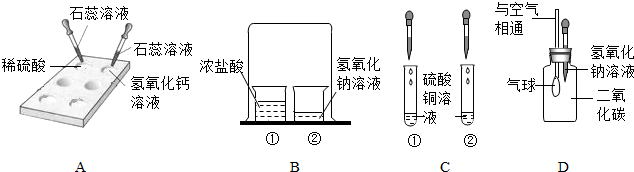
(1)在白色点滴板上完成实验A,请将实验现象补充完整.
(2)在实验B的烧杯②中滴加2滴酚酞溶液后,扣上大烧杯,一段时间后看到的现象是氢氧化钠溶液由红色变成无色,得出的结论是浓盐酸具有挥发性,酸碱会发生中和反应.
(3)在实验C的试管①中,滴加少量的氢氧化钠溶液,看到的现象是有蓝色沉淀生成,反应的化学方程式是2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.要使试管②中产生白色沉淀,应滴加氯化钡溶液(写一种溶液).
(4)小亮用实验D验证二氧化碳与氢氧化钠溶液反应,看到的现象是气球胀大,他根据三氧化硫与二氧化碳所属的类别,推断三氧化硫也能与氢氧化钠溶液反应,反应的化学方程式为SO3+2NaOH=Na2SO4+H2O.

(1)在白色点滴板上完成实验A,请将实验现象补充完整.
| 稀硫酸 | 氢氧化钙溶液 | |
| 实验现象 | 溶液变红色 | 溶液变蓝色 |
(3)在实验C的试管①中,滴加少量的氢氧化钠溶液,看到的现象是有蓝色沉淀生成,反应的化学方程式是2NaOH+CuSO4=Cu(OH)2↓+Na2SO4.要使试管②中产生白色沉淀,应滴加氯化钡溶液(写一种溶液).
(4)小亮用实验D验证二氧化碳与氢氧化钠溶液反应,看到的现象是气球胀大,他根据三氧化硫与二氧化碳所属的类别,推断三氧化硫也能与氢氧化钠溶液反应,反应的化学方程式为SO3+2NaOH=Na2SO4+H2O.