题目内容
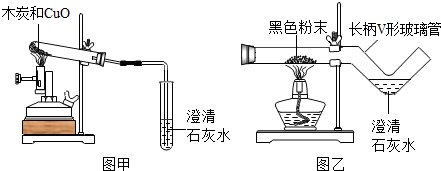
我国劳动人民早在五千年前就会使用木炭炼铜.在化学实验室里模拟炼铜,既可用传统的实验装置(见图甲),又能用改进的微型实验装置(见图乙).化学兴趣小组采用图乙装置,开展以下探究活动.
(1)写出木炭与CuO反应的化学方程式: ,失去氧原子的物质是 ,发生了 反应.氧化剂还原剂都属于 物(反应物或生成物).
(2)判断木炭与CuO已经发生化学反应的依据是 .
(3)使用图乙装置与使用图甲装置相比,其优点是 (写出1条即可).
(4)用甲装置进行实验,完毕后先停止加热,可能会引起的后果是 .
(5)澄清石灰水中含有的氢氧化钙属于 (填酸、碱、盐或氧化物),澄清石灰水也参与了化学反应,在反应中逐渐变成了 (填溶液、乳浊液或悬浊液).

(1)写出木炭与CuO反应的化学方程式:
(2)判断木炭与CuO已经发生化学反应的依据是
(3)使用图乙装置与使用图甲装置相比,其优点是
(4)用甲装置进行实验,完毕后先停止加热,可能会引起的后果是
(5)澄清石灰水中含有的氢氧化钙属于
考点:碳的化学性质,悬浊液、乳浊液的概念及其与溶液的区别,常见的氧化物、酸、碱和盐的判别,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)根据反应的过程来进行分析;
(2)根据实验中发生的现象来分析;
(3)微型实验装置药品用量较少,节约药品;
(4)根据实验过程中的注意事项来分析;
(5)根据化合物的分类以及物质的溶解性来分析.
(2)根据实验中发生的现象来分析;
(3)微型实验装置药品用量较少,节约药品;
(4)根据实验过程中的注意事项来分析;
(5)根据化合物的分类以及物质的溶解性来分析.
解答:解:(1)在高温的条件下,碳和氧化铜反应生成铜和二氧化碳,其中氧化铜失去氧发生了还原反应,碳得到氧发生了氧化反应,氧化铜是氧化剂、碳是还原剂,均为反应物;
(2)碳和氧化铜均为黑色,铜是红色的,生成的二氧化碳能使澄清的石灰水变浑浊,均证明发生了化学反应;
(3)微型实验装置药品用量较少,节约药品,现象明显,操作简单;
(4)用甲装置进行实验,完毕后先停止加热,会导致液体到吸入试管,而造成试管的炸裂;
(5)氢氧化钙是由钙离子和氢氧根离子构成的化合物,属于碱,二氧化碳与氢氧化钙反应生成碳酸钙难溶于水,形成了悬浊液.
故答案为:(1)C+2CuO
2Cu+CO2↑;CuO;还原;反应物;
(2)黑色固体中逐渐有红色固体产生,澄清的石灰水变浑浊;
(3)操作简单;
(4)液体倒流,引起试管爆裂;
(5)碱;悬浊液.
(2)碳和氧化铜均为黑色,铜是红色的,生成的二氧化碳能使澄清的石灰水变浑浊,均证明发生了化学反应;
(3)微型实验装置药品用量较少,节约药品,现象明显,操作简单;
(4)用甲装置进行实验,完毕后先停止加热,会导致液体到吸入试管,而造成试管的炸裂;
(5)氢氧化钙是由钙离子和氢氧根离子构成的化合物,属于碱,二氧化碳与氢氧化钙反应生成碳酸钙难溶于水,形成了悬浊液.
故答案为:(1)C+2CuO
| ||
(2)黑色固体中逐渐有红色固体产生,澄清的石灰水变浑浊;
(3)操作简单;
(4)液体倒流,引起试管爆裂;
(5)碱;悬浊液.
点评:有关实验方案的设计和对实验方案的评价是中考的热点之一,设计实验方案时,要注意用最少的药品和最简单的方法;关于对实验设计方案的评价,要在两个方面考虑,一是方案是否可行,能否达到实验目的;二是设计的方法进行比较,那种方法更简便.本考点主要出现在实验题中.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验操作不能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去混入氮气中的氧气 | 通过炽热的铜网 |
| B | 检验二氧化碳中含有少量的一氧化碳 | 点燃 |
| C | 鉴别氯化钙和碳酸钙 | 加入足量的水 |
| D | 检验黄铜中含有锌 | 加入稀盐酸 |
| A、A | B、B | C、C | D、D |
在一密闭容器中盛有等质量的木炭和氧气,高温加热使之充分反应后,容器内的物质主要是( )
| A、CO |
| B、CO2和O2 |
| C、CO和木炭 |
| D、CO2 |
小明在资料中找到下列微粒的结构示意图,请你分析以下的叙述中正确的是( )
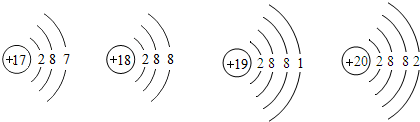

| A、上述各微粒中,最外层电子数都没有达到稳定结构 |
| B、核电荷数为18的微粒是失电子后形成的阴离子 |
| C、原子序数为19的元素的金属活动性,比原子序数为20的元素的金属活动性强 |
| D、质子数为17、18的微粒都属于易得电子的非金属元素 |


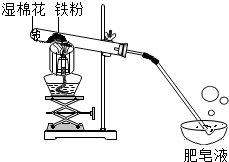 常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物.
常温下没有氧气存在时,铁与水几乎不反应,但高温下,铁与水蒸气能反应生成一种常见铁的氧化物和一种气体.小明很好奇,设计如下实验探究铁粉与水蒸气反应后的产物. 碳元素是组成许多物质的基本元素,按要求回答相关问题:
碳元素是组成许多物质的基本元素,按要求回答相关问题:
 已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易于血液中血红蛋白结合的有毒气体.它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答:(1)写出E、B的化学式:E
已知A、B、C三种物质含有同种金属元素,其中A是大理石的主要成分,B为氧化物;D、E、F三种物质含有同种非金属元素,其中F是单质,E是易于血液中血红蛋白结合的有毒气体.它们之间的转化关系如图所示(有些转换关系,反应条件等略去),试回答:(1)写出E、B的化学式:E