题目内容
我市某校初三某班学生去春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量(g) | 20.0 | 30.0 | 40.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 2.0 | 1.0 |
(1)10.0g样品与______g盐酸恰好完全反应.
(2)样品中碳酸钙的质量分数是______.
(3)所用稀盐酸的溶质的质量分数是多少?
②由题意和图表可知,完全反应后剩余固体是杂质,质量为1.0g,据此计算出石灰石样品中碳酸钙的质量,然后根据质量分数公式可计算出样品中碳酸钙的质量分数;
(2)根据碳酸钙与盐酸反应的化学方程式和CaCO3的质量,列出比例式,就可计算出生成二氧化碳的质量.
解答:解:
(1)①由图表可知,四位同学所取样品的质量相等,每增加10.0g盐酸固体的质量减少2g;而丁同学加入 50.0g盐酸与10.0g样品反应,固体质量只减少了1g,说明50.0g盐酸未完全反应,只反应了45.0g;
故答案为:45.0;
②样品中碳酸钙的质量分数为:
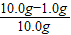 ×100%=90.0%;
×100%=90.0%;故答案为;90.0%;
(2)分析图表可知,甲、乙、丙三位同学所用盐酸均完全反应,且四位同学用的是质量分数相同的盐酸,故可用此三组数据来计算盐酸的质量分数,以甲同学所测数据计算
反应中减少的固体的质量是碳酸钙的质量,设所用稀盐酸的溶质的质量为x,
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 73
4.0g x
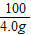 =
=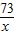
x=2.92g
所用稀盐酸的溶质的质量分数是:
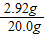 ×100%=14.6%
×100%=14.6%答:所用稀盐酸的溶质的质量分数是14.6%.
点评:本题主要考查学生分析图表寻找相关信息,以及利用化学方程式进行计算的能力,能较好考查学生分析和解决实际问题的能力,是中考的常考题型.

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案我市某校初三某班学生去春游,带回了几小块石灰石样品.为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量(g) | 20.0 | 30.0 | 40.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 2.0 | 1.0 |
(1)10.0g样品与______g盐酸恰好完全反应.
(2)样品中碳酸钙的质量分数是______.
(3)所用稀盐酸的溶质的质量分数是多少?
我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品。为了测定样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石 样品质量/g | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸 的质量/g | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体 的质量/g | 6.0 | 4.0 | 1.0 | 1.0 |
试回答:
(1)10.0 g样品与45 g盐酸充分反应后,盐酸是否还剩余________(填“是”或“否”),样品中碳酸钙的质量分数是________。
(2)10.0 g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程,计算结果精确到小数点后两位)
(7分)我市某校初三(1)班学生去湖光岩春游,带回了几小块石灰石样品。为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用质量分数相同的盐酸与样品充分反应来讲行实验测定,(样品中的杂质不溶于水,且不与盐酸反应),测得数据如下表:
| 甲同学 | 乙同学 | 丙同学 | 丁同学 | |
| 所取石灰石样品质量(g) | 10.0 | 10.0 | 10.0 | 10.0 |
| 加入盐酸的质量(g) | 20.0 | 30.0 | 45.0 | 50.0 |
| 剩余固体的质量(g) | 6.0 | 4.0 | 1.0 | 1.0 |
试问答:
(1)10.0g样品与45g盐酸充分反应后,盐酸是否还剩余_____ _____ (填“是”或“否”),样品中碳酸钙的质量分数是_______________。
(2)10.0g样品与足量稀盐酸反应后可产生二氧化碳多少克?(写出计算过程,计算结果精确到小数点后两位)