题目内容
14.向34g过氧化氢溶液中加入0.5g二氧化锰,经测定反应完全后剩余混合物的质量为33.7g(1)反应中生成氧气的质量为0.8g;
(2)计算过氧化氢溶液中溶质的质量?(写出计算过程)
分析 (1)根据质量守恒定律反应前后减少的质量即为氧气的质量;
(2)根据氧气的质量和化学方程式可求得过氧化氢的质量.
解答 解:(1)二氧化锰的质量是0.5g,则生成的气体的质量为:34.0g+0.5g-33.7g=0.8g
(2)设产生0.8g氧气需要过氧化氢的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 0.8g
$\frac{68}{x}$=$\frac{32}{0.8g}$
解得:x=1.7g
答:参加反应的过氧化氢的质量为1.7g
故答案为:
(1)0.8g;
(2)1.7g.
点评 在解此类题时,首先利用质量守恒定律解出氧气的质量,然后利用方程式中的比例关系解出需要求解的物质的质量.

练习册系列答案
 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案
相关题目
15.下列变化中,能证明分子在化学变化中可分的是( )
| A. | 氧化汞受热生成汞和氧气 | B. | 分离液态空气制氧气 | ||
| C. | 水加热变成水蒸气 | D. | 石蜡受热熔化 |
5.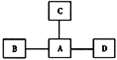 通常将纯净物分成单质、氧化物、酸、碱、盐等类别,从类别的角度来研究它们的性质及反应.
通常将纯净物分成单质、氧化物、酸、碱、盐等类别,从类别的角度来研究它们的性质及反应.
(1)已知初中化学常见的七种物质A-G,所属物质类别和组成元素的种类如下表.
其中A、B均能与C反应,A与C反应的生成物所含两种元素的质量比是3:2; B与C反应的生成物组成元素与E相同;C与D反应的生成物常温下为液态,其组成元素与F相同;A、B均能与G溶液反应,且反应后所得溶液的质量均増加.则E的化学式是Fe2O3;F所含的元素是氢和氧.
以下反应的化学方程式分别是:①B+C3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;②C+D2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;③A+GMg+H2SO4=MgSO4+H2↑.
(2)A、B、C、D均为初中常见物质,转化关系如图所示.
①若A能由其他三种物质转化而成,这四种物质分别是单质、氧化物、酸、碱、盐中的一种,且均含有一种相同元素.其中A是一种温室气体,则其他三种物质的化学式分别是O2、H2SO4、CaCO3.
②若A与其他三种物质均能相互转化,A是地球上含量最多的无色液体,A、B、C、D的相对分子质量依次增大.则C的化学式是H2CO3,D转化成A的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O.
 通常将纯净物分成单质、氧化物、酸、碱、盐等类别,从类别的角度来研究它们的性质及反应.
通常将纯净物分成单质、氧化物、酸、碱、盐等类别,从类别的角度来研究它们的性质及反应.(1)已知初中化学常见的七种物质A-G,所属物质类别和组成元素的种类如下表.
| 物质分类 | 单质 | 化合物 | ||
| 元素种类 | 金属 | 非金属 | 两种 | 三种 |
| 物质代号 | A、B | C、D | E、F | G |
以下反应的化学方程式分别是:①B+C3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;②C+D2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;③A+GMg+H2SO4=MgSO4+H2↑.
(2)A、B、C、D均为初中常见物质,转化关系如图所示.
①若A能由其他三种物质转化而成,这四种物质分别是单质、氧化物、酸、碱、盐中的一种,且均含有一种相同元素.其中A是一种温室气体,则其他三种物质的化学式分别是O2、H2SO4、CaCO3.
②若A与其他三种物质均能相互转化,A是地球上含量最多的无色液体,A、B、C、D的相对分子质量依次增大.则C的化学式是H2CO3,D转化成A的化学方程式是Ca(OH)2+2HCl=CaCl2+2H2O.
2.下列实验基本操作正确的是( )
| A. | 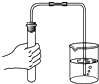 | B. | 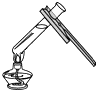 | C. | 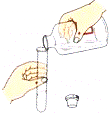 | D. | 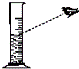 |
9.下列做法中,不正确的是( )
| A. | 点燃氢气前,一定要先检验氢气的纯度 | |
| B. | 将固体溶解的时候要用玻璃棒不断的搅拌 | |
| C. | 把氢氧化钠固体放在天平左盘的玻璃器皿中称量 | |
| D. | 浓硫酸沾到皮肤上,立即用大量水冲洗,再涂上硼酸溶液 |
3.某学生用托盘天平称量10.4克药品,天平调平衡后,进行称量时发现指针向左偏,他应该( )
| A. | 增加药品 | B. | 减少药品 | C. | 拨动游码 | D. | 调节平衡螺母 |
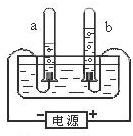 实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题:
实验是化学学习的一种重要手段,如利用电解水实验可探究水的组成.请根据电解水实验回答下列问题: