题目内容
8.金属与我们的生活息息相关,用途广泛.(1)将不锈钢制成金属丝与棉纤维一起织成防护服,这利用了不锈钢的B(填序号)
A.耐腐蚀性 B.延展性 C.导热性 D.导电性
(2)血液中缺乏亚铁离子会造成贫血,某麦片中含微量铁粉,在胃酸作用下转化为人体可吸收的铁元素,该反应的方程式为Fe+2HCl═FeCl2+H2↑,这种麦片必须真空保存的原因是铁能和水、氧气反应生成铁锈.
(3)某化学小组为他探究锌、铁、铜三种金属的活动性顺序,设计了如图所示的两个实验:
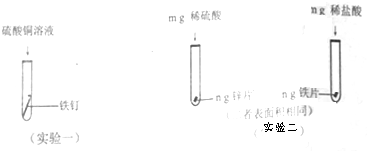
①实验一种,若出现铁钉表面附着一层红色固体现象,可证明铁的活动性强于铜.
②实验二中,小明以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为不够严谨,理由是利用的不是同种酸.
分析 (1)不锈钢可以制成金属丝,说明不锈钢具有良好的延展性;
(2)铁能和胃液中的稀盐酸反应生成氯化亚铁和氢气;
铁能和空气中的水、氧气反应生成铁锈;
(3)铁能和硫酸铜反应生成硫酸亚铁和铜;
对比试验要确定好常量和变量.
解答 解:(1)将不锈钢制成金属丝与棉纤维一起织成防护服,这利用了不锈钢的延展性.
故填:B.
(2)铁和稀盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑;
这种麦片必须真空保存的原因是铁能和水、氧气反应生成铁锈.
故填:Fe+2HCl═FeCl2+H2↑;铁能和水、氧气反应生成铁锈.
(3)①实验一种,若铁钉表面附着一层红色固体,可证明铁的活动性强于铜.
故填:铁钉表面附着一层红色固体.
②实验二中,利用的酸分别是稀硫酸和稀盐酸,无法比较锌、铁的活动性强弱.
故填:利用的不是同种酸.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
3.近代化学工业是从无机化学产品的生产起步的,特别是“三酸两碱”--硫酸、盐酸、硝酸、纯碱、烧碱.下列关于“三酸两碱”说法错误的是( )
| A. | 纯碱溶液pH>7 | B. | 浓硫酸、浓盐酸可作干燥剂 | ||
| C. | 盐酸可用于除锈 | D. | 硝酸能与烧碱发生中和反应 |
13.等质量的CO和CO2中所含氧元素质量之比是( )
| A. | 1:1 | B. | 14:11 | C. | 11:14 | D. | 11:7 |
18.“金银铜铁锡”俗称五金口在这五种金属中,金属活动生最弱的是( )
| A. | 铁 | B. | 铜 | C. | 金 | D. | 银 |
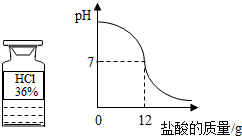 某同学在实验室看到一瓶久置的盐酸,为测定其试剂的溶质质量分数,在烧杯中加入20g溶质质量分数为20%的氢氧化钠溶液,逐滴加入该盐酸,pH测定仪记录了加入盐酸的质量与烧杯中溶液的pH关系(如图所示).
某同学在实验室看到一瓶久置的盐酸,为测定其试剂的溶质质量分数,在烧杯中加入20g溶质质量分数为20%的氢氧化钠溶液,逐滴加入该盐酸,pH测定仪记录了加入盐酸的质量与烧杯中溶液的pH关系(如图所示).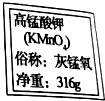 某同学准备用高锰酸钾制取氧气,他取出没开封的高锰酸钾试剂.看到瓶上标签如图所示.
某同学准备用高锰酸钾制取氧气,他取出没开封的高锰酸钾试剂.看到瓶上标签如图所示.