题目内容
 某化学小组用如图所示的装置测定空气中氧气的含量,硬质玻璃管内装有细铜丝,且两个注射器组成的密闭系统内留有50mL室温下的空气.对该实验的认识不正确的是( )
某化学小组用如图所示的装置测定空气中氧气的含量,硬质玻璃管内装有细铜丝,且两个注射器组成的密闭系统内留有50mL室温下的空气.对该实验的认识不正确的是( )| A、若实验很成功,出现的现象是细铜丝由紫红色变为黑色 |
| B、若实验很成功,冷却后,密闭容器内气体的体积约为40mL |
| C、该实验不能证明空气是混合物 |
| D、加热过程中,交替缓慢推动两注射的目的是使空气中的氧气与铜充分反应 |
考点:空气组成的测定
专题:空气与水
分析:分析实验原理:通过铜丝在密闭注射器里的空气中的燃烧,消耗了氧气,压强减小,注射器里的空气的减小来测定空气中氧气的体积分数.为了全部消耗掉氧气,铜丝的量必须是足量的;空气中除了氧气;剩余的气体主要是氮气,还有稀有气体、二氧化碳等,剩余的气体还是混合物;气体的体积要受温度的影响,读数时必须等到装置冷却至室温再读.
解答:解:
A、若实验很成功,出现的现象是细铜丝由紫红色变为黑色,故A正确;
B、空气中氧气的体积分数约占空气体积的21%,则若实验很成功,冷却后,密闭容器内气体的体积约为40mL,故B错误;
C、空气中除了氧气,还有剩余的气体,故“该实验能证明空气是混合物”,故C错误;
D、在实验的加热过程中,交替缓慢推动两注射器的目的是 使空气中的氧气与铜充分反应,故D正确.
故选:C.
A、若实验很成功,出现的现象是细铜丝由紫红色变为黑色,故A正确;
B、空气中氧气的体积分数约占空气体积的21%,则若实验很成功,冷却后,密闭容器内气体的体积约为40mL,故B错误;
C、空气中除了氧气,还有剩余的气体,故“该实验能证明空气是混合物”,故C错误;
D、在实验的加热过程中,交替缓慢推动两注射器的目的是 使空气中的氧气与铜充分反应,故D正确.
故选:C.
点评:本题考查了通过铜丝在密闭注射器里的空气中的燃烧测定了空气中氧气的体积分数.通过设计一些定量实验探究,可培养学生的开放性思维,使学生会对所学的化学原理进行综合应用.

练习册系列答案
相关题目
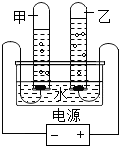 用如图所示的装置进行电解水实验,有以下描述:
用如图所示的装置进行电解水实验,有以下描述:①向水中加入少量硫酸,能使水电解产生气体的速度变大;
②甲、乙两试管内收集到的气体的体积约为2:1;
③甲试管内产生的气体能燃烧;
④乙试管内产生的气体能使带火星的木条复燃.以上描述中正确的是( )
| A、①②③④ | B、③ |
| C、①② | D、①②③ |
某反应的微观示意图如图(一种小球代表一种元素的原子),下列说法错误的是( )

| A、该反应中共有三种元素 |
| B、图中反应物都是化合物 |
| C、该反应的本质是原子的重新组合 |
| D、该反应前后分子的种类发生改变 |
下列各组实验用品,不能用于锌和铁的金属活动性强弱的是( )
| A、铁丝、硫酸锌溶液 |
| B、锌片、铁片、硫酸镁溶液 |
| C、锌片、硫酸亚铁溶液 |
| D、锌片、铁片、稀硫酸 |
夏天来了,旅游的人们把目光放入了大自然的群山中,投人群山的怀抱固然美好,可是我们要时刻注意保护森林,安全防火,下列标志中与安全防火有关的是( ) 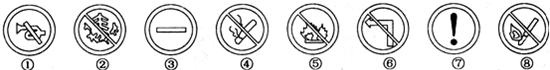

| A、①②③④ | B、④⑤⑥⑦ |
| C、②④⑤⑧ | D、①③⑥⑦ |
某学生用量筒取液体时,将量筒放平,倒入液体,面对刻度线,第一次仰视凹液面最低处,读数为19毫升;倒出部分液体,又俯视液面最低处,读数为11毫升,该学生倒出的液体的体积是( )
| A、8毫升 | B、大于8毫升 |
| C、小于8毫升 | D、无法判断 |