题目内容
3.已知一个质子数和中子数都为6的碳原子的质量是1.993×10-26千克,氧原子的相对原子质量为16,则一个氧原子的质量是( )| A. | 16克 | B. | 16 | ||
| C. | 12×16×1.993×10-26千克 | D. | 16×1.993×10-26千克/12 |
分析 根据某原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$,结合题意进行分析解答即可.
解答 解:一个质子数和中子数都为6的碳原子的质量是1.993×10-26千克,氧原子的相对原子质量为16,设一个氧原子的质量是x,
则$\frac{x}{1.993×1{0}^{-26}kg×\frac{1}{12}}$=16,x=16×1.993×10-26千克×$\frac{1}{12}$.
故选:D.
点评 本题难度不大,掌握原子的相对原子质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$并能灵活运用是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
13.下列四个图象中,反映出的对应变化关系错误的是( )
| A. | 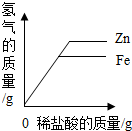 将等质量的锌片和铁片分别加入足量的等质量等质量分数的稀盐酸中 | |
| B. |  一定温度下,向接近饱和的硝酸钾溶液中不断加入硝酸钾固体 | |
| C. | 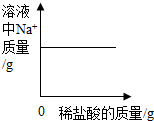 向一定量的氢氧化钠溶液中滴加稀盐酸 | |
| D. | 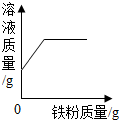 向一定量的硫酸铜溶液中加入铁粉 |
18.某探究性活动中,甲、乙同学设计并完成了如图所示的实验.

①写出甲同学实验中发生反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O.
②反应结束后,甲、乙同学把废液倒入同一废液缸中,观察到废液缸中产生少量的气泡,最终有白色沉淀生成.请回答以下问题:
(I)废液缸中最终生成的白色沉淀是碳酸钙.
(II)甲同学实验后的废液中一定含有的溶质是HCl、CaCl2.
③丙同学从实验②的废液缸中取出废液,过滤,对滤液进行了探究.请你帮助丙同学完成以下探究方案:
【探究结论】该滤液中含有的溶质是Na2CO3和NaCl.

①写出甲同学实验中发生反应的化学方程式Ca(OH)2+2HCl=CaCl2+2H2O.
②反应结束后,甲、乙同学把废液倒入同一废液缸中,观察到废液缸中产生少量的气泡,最终有白色沉淀生成.请回答以下问题:
(I)废液缸中最终生成的白色沉淀是碳酸钙.
(II)甲同学实验后的废液中一定含有的溶质是HCl、CaCl2.
③丙同学从实验②的废液缸中取出废液,过滤,对滤液进行了探究.请你帮助丙同学完成以下探究方案:
| 探究目的 | 探究步骤 | 实验现象 |
| 检验滤液中有Na2CO3 | A.取少量滤液于试管中,滴加过量的稀硝酸 | 产生气泡 |
| 检验滤液中有NaCl | B.向实验A所得溶液中滴加硝酸银溶液 | 产生白色沉淀 |
8.在生产和生活中,使用硬水会带来许多危害.下列说法不正确的是( )
| A. | 生活中可以采用煮沸的方法软化硬水 | |
| B. | 过滤和吸附能将硬水转变成软水 | |
| C. | 雨水、蒸馏水均属于软水 | |
| D. | 可用肥皂水鉴别硬水,产生的泡沫较少 |
12.下列有关说法正确的是( )
| A. | 摩尔是国际单位制中七个基本物理量之一 | |
| B. | 1mol H2约含6.02×1023个氢原子 | |
| C. | 1molSO2比1molSO3少1个氧原子 | |
| D. | 1 molCO和1 molCO2所含碳元素质量相等 |