题目内容
3.大蒜中含有“硫化丙烯”,其化学式为C3H6S,能杀菌,具有一定的抗病功能和食疗价值.下列关于硫化丙烯的说法中正确的是( )| A. | 硫化丙烯中氢元素质量分数最大 | |
| B. | 硫化丙烯分子是保持硫化丙烯化学性质的最小粒子 | |
| C. | 硫化丙烯由3个碳原子、6个氢原子、1个硫原子构成 | |
| D. | 硫化丙烯中碳元素、氢元素、硫元素的质量比为3:6:1 |
分析 A.根据化合物中元素的质量比来分析;
B.根据物质的构成以及分子的概念来分析;
C.根据物质的结构来分析;
D.根据化合物中元素的质量比来分析.
解答 解:A.根据化合物中各元素质量比=各元素的相对原子质量×原子个数之比,所以硫化丙烯中碳、氢、硫三种元素的质量比为(12×3):(1×6):32=18:3:16,可见其中氢元素的质量分数最小,故错误;
B.分子是保持物质化学性质的最小粒子,硫化丙烯是由分子构成的,故硫化丙烯分子是保持硫化丙烯化学性质的最小粒子,故正确;
C.硫化丙烯是由分子构成的,而不是由原子直接构成的,故错误;
D.硫化丙烯中碳、氢、硫三种元素的质量比为(12×3):(1×6):32=18:3:16,故错误.
故选B.
点评 本题主要考查化学式的意义及计算,根据化学式确定其元素组成及组成物质元素之间的质量关系,掌握了这些问题就不难解决此题了.

练习册系列答案
相关题目
13.为确定某大理石样品的纯度,某兴趣小组进行如下实验:称取该大理石(杂质不参加反应)加入烧杯中,向其中逐渐加入稀盐酸至完全反应.反应结束后,称量烧杯及其中物质的总质量(溶解的气体忽略不计),有关数据记录如表.
(1)实验中产生的二氧化碳质量为3.3g.
(2)求该大理石的纯度.(写出计算过程,计算结果精确到0.1%)
(3)实验中若用浓盐酸代替稀盐酸,会使实验结果偏大,原因是浓盐酸有挥发性,会导致测得的二氧化碳质量偏高,从而导致计算所得的碳酸钙质量偏大,最终导致实验结果偏大.
| 烧杯 | 大理石 | 稀盐酸 | 反应后烧杯及其中物质总质量 | |
| 质量(克) | 90 | 8.5 | 50 | 145.2 |
(2)求该大理石的纯度.(写出计算过程,计算结果精确到0.1%)
(3)实验中若用浓盐酸代替稀盐酸,会使实验结果偏大,原因是浓盐酸有挥发性,会导致测得的二氧化碳质量偏高,从而导致计算所得的碳酸钙质量偏大,最终导致实验结果偏大.
11.鱼能在水中生存是因为( )
| A. | 水中含有氧元素 | B. | 水中溶解有氧分子 | ||
| C. | 水中有氧原子 | D. | 水可以分解生成氧气和氢气 |
12.下列说法正确的是( )
| A. | 可燃冰就是干冰,主要成分为CO2 | |
| B. | 乙醇是一种很好的燃料,属于不可再生能源 | |
| C. | 点燃氢气前一定要检验其纯度 | |
| D. | 化石燃料主要包括煤、石油、天然气,属于可再生能源 |

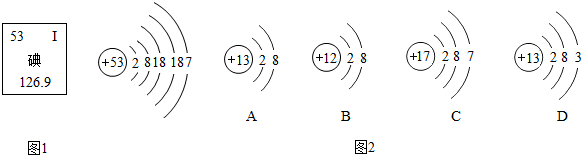
 ,当a=10时,该粒子是原子;当a=11时,该粒子的符号为Na+.
,当a=10时,该粒子是原子;当a=11时,该粒子的符号为Na+.




 2016年10月17日,神舟十一号载人飞船发生成功.2016年11月19日凌晨,神舟十一号飞船与天宫二号自动交汇对接成功;11月18日,神舟十一号返回舱顺利着陆.请回答下列相关问题:
2016年10月17日,神舟十一号载人飞船发生成功.2016年11月19日凌晨,神舟十一号飞船与天宫二号自动交汇对接成功;11月18日,神舟十一号返回舱顺利着陆.请回答下列相关问题: