题目内容
11.某黑色固体A和液体B生成液体C和气体D,而A在反应前后质量和化学性质都没有发生改变,将红褐色固体粉末E加热后放在D物质里能剧烈燃烧,有大量的白烟F生成.试判断:A是:过氧化氢溶液、D是:氧气、F是:五氧化二磷.分析 根据红褐色固体粉末E加热后放在D物质里能剧烈燃烧,有大量的白烟F生成,所以D具有助燃性,D是氧气,E是红磷,红磷和氧气反应生成五氧化二磷,所以F是五氧化二磷,黑色固体A和液体B生成液体C和氧气,而A在反应前后质量和化学性质都没有发生改变,结合实验室制取氧气的药品和方法可知,A是二氧化锰,B是过氧化氢溶液,C是水,然后将推出的物质进行验证即可.
解答 解:红褐色固体粉末E加热后放在D物质里能剧烈燃烧,有大量的白烟F生成,所以D具有助燃性,D是氧气,E是红磷,红磷和氧气反应生成五氧化二磷,所以F是五氧化二磷,黑色固体A和液体B生成液体C和氧气,而A在反应前后质量和化学性质都没有发生改变,结合实验室制取氧气的药品和方法可知,A是二氧化锰,B是过氧化氢溶液,C是水,经过验证,推导正确,所以A是过氧化氢溶液,D是氧气,F是五氧化二磷.
故答案为:过氧化氢溶液,氧气,五氧化二磷.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
1.小明同学看到妈妈把买来的排水口洗净剂(主要成分:过碳酸钠、柠檬酸)洒在厨房排水口网状盖的底部,倒上温水后迅速冒出气泡.为了解其反应过程,他与学习小组的同学进行了如下探究.

【活动探究一】教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:
【提出问题1】无色溶液X中的溶质有哪些物质?
【猜想与假设】根据以上实验现象,无色溶液X中一定存在的溶质是H2O2.
根据质量守恒定律,同学们对溶液X中还可能存在其它溶质,作出如下猜想:
①Na2CO3;②NaHCO3;③Na2CO3和 NaHCO3的混合物.
【查阅资料】
【实验探究】为了确定溶液X还可能存在的其它溶质,设计如下方案,请你一起完成.
【反思】实验步骤①中,氯化钙溶液过量的目的是除尽碳酸钠溶液,避免对碳酸氢钠溶液检验的干扰.
【活动探究二】
提出问题2:如何测量Na2CO3和NaHCO3的固体混合物中各成分的质量?
(1)为测量混合物中各成分的质量,小明设计了图1装置.通过称量B装置的质量变化来确定样品中各成分的质量.该装置气密性良好,稀硫酸与样品、进入装置B的CO2与NaOH均完全反应,操作无误.但多次发现,测定结果有偏差.造成偏差的原因有:①成的二氧化碳气体没有全部被氢氧化钠浓溶液吸收;②氢氧化钠浓溶液还吸收到了空气中的二氧化碳气体.
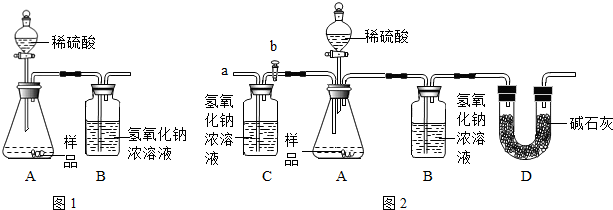
(2)在老师的指导下小明重新设计了图2的实验装置进行实验.小明取9.5g固体样品进行实验,实验完毕后测得B装置增重4.4g,则样品中各成分的质量分别为多少?(写出计算过程,计算结果保留一位小数.)
(可能用到的相对分子质量:Na2CO3:106,NaHCO3:84,CO2:44)

【活动探究一】教师提供了一瓶过碳酸钠(Na2CO4),小组同学进行了如下实验探究:
【提出问题1】无色溶液X中的溶质有哪些物质?
【猜想与假设】根据以上实验现象,无色溶液X中一定存在的溶质是H2O2.
根据质量守恒定律,同学们对溶液X中还可能存在其它溶质,作出如下猜想:
①Na2CO3;②NaHCO3;③Na2CO3和 NaHCO3的混合物.
【查阅资料】
| NaHCO3溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 产生气泡 |
| 加入饱和石灰水 | 溶液变浑浊 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
| 加热溶液至沸腾, 将气体通入澄清石灰水 | 澄清石灰水变浑浊 | 澄清石灰水无明显变化 |
| 步骤 | 现象 | 结论与方程式 |
| ①取少量溶于水,加入过量CaCl2溶液. | 产生白色沉淀 | 该反应方程式: CaCl2+Na2CO3═CaCO3↓+2NaCl. |
| ②将上述反应后混合液过滤,取滤液 稀盐酸. | 有气泡冒出 | 证明猜想③成立. |
【活动探究二】
提出问题2:如何测量Na2CO3和NaHCO3的固体混合物中各成分的质量?
(1)为测量混合物中各成分的质量,小明设计了图1装置.通过称量B装置的质量变化来确定样品中各成分的质量.该装置气密性良好,稀硫酸与样品、进入装置B的CO2与NaOH均完全反应,操作无误.但多次发现,测定结果有偏差.造成偏差的原因有:①成的二氧化碳气体没有全部被氢氧化钠浓溶液吸收;②氢氧化钠浓溶液还吸收到了空气中的二氧化碳气体.

(2)在老师的指导下小明重新设计了图2的实验装置进行实验.小明取9.5g固体样品进行实验,实验完毕后测得B装置增重4.4g,则样品中各成分的质量分别为多少?(写出计算过程,计算结果保留一位小数.)
(可能用到的相对分子质量:Na2CO3:106,NaHCO3:84,CO2:44)
2.某元素的化合价只有一种,它的氧化物的化学式为R2O3,则R的下列化合物中化学式正确的是( )
| A. | R2Cl2 | B. | R2(SO4)3 | C. | RNO3 | D. | R2(OH)3 |
19.下列物质中属于氧化物的是( )
| A. | H2SO4 | B. | KOH | C. | CO | D. | KClO3 |
6.用扇子一扇,燃着的蜡烛立即熄灭,其原因是( )
| A. | 供给的氧气减少 | B. | 供给氧气增加 | ||
| C. | 蜡烛的着火点降低 | D. | 烛心温度低于着火点 |
20.下列化肥中,属于复合肥料的是( )
| A. | CO(NH2)2 | B. | NH4NO3 | C. | KNO3 | D. | Ca(H2PO4)2 |