题目内容
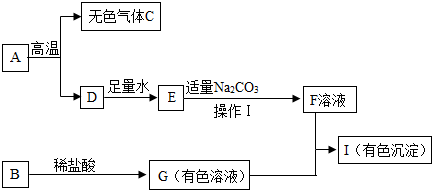
11.氨碱法制纯碱的工业流程如下:
(1)最终所得纯碱主要成分的化学式是Na2CO3,它属于盐(填“酸”“碱”或“盐”),该产品易溶于水,溶液显碱性.
(2)由步骤③所得的碳酸氢钠在生产和生活中有许多重要用途,在医疗上,它是治疗胃酸过多的药剂之一.
(3)试写出步骤 ④中发生反应的化学方程式2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
分析 (1)根据向饱和食盐水中加入氨气、二氧化碳后,能够生成碳酸氢钠和氯化铵,相同条件下碳酸氢钠的溶解度小于氯化铵的溶解度,因此碳酸氢钠会析出,加热碳酸氢钠能够生成碳酸钠、水和二氧化碳,从而得到纯碱进行分析;
(2)根据碳酸氢钠能和稀盐酸反应生成氯化钠、水和二氧化碳进行分析;
(3)根据碳酸氢钠在加热的条件下生成碳酸钠、水和二氧化碳进行分析.
解答 解:(1)最终所得纯碱的主要成分是碳酸钠,碳酸钠的化学式是Na2CO3,碳酸钠是由钠离子和碳酸根离子组成的化合物,属于盐,碳酸钠溶于水时溶液显碱性;
(2)碳酸氢钠无毒,能够和胃液中的稀盐酸反应,因此可以用于治疗胃酸过多;
(3)碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,化学方程式为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑.
故答案为:(1)Na2CO3,盐,碱;
(2)胃酸;
(3)2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
点评 化学来源于生产、生活,也服务于生产、生活,要学好化学知识,为生产、生活服务.

练习册系列答案
 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案
相关题目
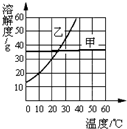
6. 将10.0%的NaOH溶液逐滴加入到50g稀盐酸中,得到混合液的温度与加入NaOH溶液的质量关系如图.下列说法正确的是( )
将10.0%的NaOH溶液逐滴加入到50g稀盐酸中,得到混合液的温度与加入NaOH溶液的质量关系如图.下列说法正确的是( )
 将10.0%的NaOH溶液逐滴加入到50g稀盐酸中,得到混合液的温度与加入NaOH溶液的质量关系如图.下列说法正确的是( )
将10.0%的NaOH溶液逐滴加入到50g稀盐酸中,得到混合液的温度与加入NaOH溶液的质量关系如图.下列说法正确的是( )| A. | a点时的混合液能与Fe发生置换反应 | |
| B. | b点时的混合液能与Mg(NO3)2发生两种复分解反应 | |
| C. | 加入40 g NaOH溶液时混合液pH>7 | |
| D. | 稀盐酸中HCl的质量分数为7.3% |
3.分类、类比是学习化学常用的有效方法.请回答:
(1)初中化学教材中有很多实验,若按照实验目的不同来分类,可以将下表中的②③;①④(填字母)归为一类,依据是:②③都是探究反应发生的条件;①④都是探究物质的性质.
(2)在金属活动性顺序中,钙的活动性较强,不-能与活动性位于它之后的金属的盐溶液直接发生置换反应,而是先和水发生反应.已知金属钙和水反应的化学方程式为:Ca+2H2O═Ca(OH)2+H2↑.则将金属钙投入氯化铵溶液中会观察到的现象是:溶液中有气泡产生,并产生刺激性气味.试写出该过程的总反应的化学方程式Ca+2NH4Cl═CaCl2+H2↑+2NH3↑.
(1)初中化学教材中有很多实验,若按照实验目的不同来分类,可以将下表中的②③;①④(填字母)归为一类,依据是:②③都是探究反应发生的条件;①④都是探究物质的性质.
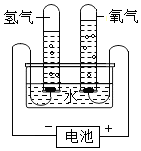 | 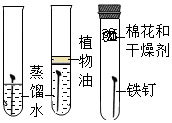 | 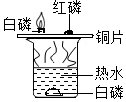 | 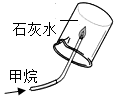 |
| ① | ② | ③ | ④ |

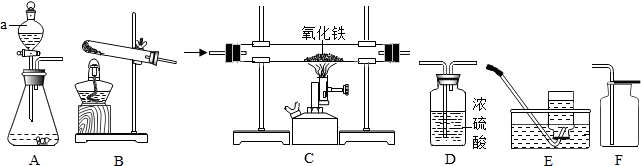
 (1)下列实验均涉及到水,其中水仅作为溶剂的是AC;
(1)下列实验均涉及到水,其中水仅作为溶剂的是AC;